题目内容
18.常温下,1mol某烷烃在光照条件下与氯气发生取代反应,若在适当的条件下,完全取代需要消耗6mol Cl2,则下列判断正确的是( )| A. | 该烷烃的分子式为C5H12 | |
| B. | 反应所生成的有机产物能直接使AgNO3溶液褪色 | |
| C. | 该烷烃的四氯代物有2种 | |
| D. | 反应容器中,一氯代物所占的物质的量分数最大 |
分析 烷烃在光照条件下下和氯气取代时,取代1mol-H消耗1mol氯气,根据消耗6mol氯气可知,此烷烃中含6个H原子,即为乙烷C2H6.氯气和乙烷发生完全取代后生成C2Cl6,是非电解质,不能电离出Cl-,据此分析.
解答 解:设此烷烃的分子式为CnH2n+2,由于烷烃在光照条件下和氯气取代时,取代1mol-H消耗1mol氯气,根据消耗6mol氯气可知,此烷烃中含6个H原子,即为2n+2=6,故n=2,即此烷烃为乙烷C2H6.
A、此烷烃为乙烷C2H6,故A错误;
B、氯气和乙烷发生完全取代后生成C2Cl6,是非电解质,不能电离出Cl-,故不能直接和硝酸银溶液反应,故B错误;
C、该烃共有6个H原子,故其四氯代物种数和二氯代物种数相同,而乙烷的二氯代物有2种,故其四氯代物也有2种,故C正确;
D、反应产物中HCl的物质的量分数最大,故D错误.
故选C.
点评 本题考查了烷烃的取代反应的规律和产物的性质,应注意的是卤代烃均为非电解质,均不能电离出氯离子,故和硝酸银不能反应.

练习册系列答案
相关题目
8.下列物质的电子式书写正确的是( )
| A. | 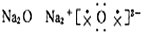 | B. | 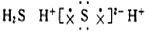 | C. | 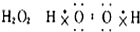 | D. | N2 N:::N |
9.在1000mL含等物质的量的HI和H2SO3的溶液里通入0.25molCl2,有二分之一的HI变为I2(已知反应:I2+H2SO3+H2O=4H++SO42-+2I-).原溶液中HI和H2SO3的浓度都等于( )
| A. | 0.2 mol•L-1 | B. | 0.1 mol•L-1 | C. | 2.0 mol•L-1 | D. | 1.0 mol•L-1 |
13.Cu2O是一种半导体材料,基于绿色化学理念设计的一制取Cu2O的电解池示意图如下,电池总反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑.下列说法正确的是( )


| A. | 石墨电极上产生氢气 | |
| B. | 铜电极被还原 | |
| C. | 铜电极接直流电源的负极 | |
| D. | 当有1 mol电子转移时,有1 mol Cu2O生成 |
3.基态原子的4s能级中只有1个电子的元素共有( )
| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 8 种 |
10.下列说法正确的是( )
| A. | 二氧化碳通入水玻璃可以得到硅酸 | |
| B. | 水泥、玻璃、陶瓷、水晶都属于硅酸盐产品 | |
| C. | 工艺师利用盐酸刻蚀石英制作艺术品 | |
| D. | 可以用澄清石灰水鉴别SO2和CO2 |
7.下列化学用语正确的是( )
| A. | 乙烯结构简式为C2H4 | B. | 乙醇的比例模型为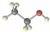 | ||
| C. | 间二甲苯的结构简式为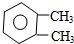 | D. | 甲烷的结构式为 |
8.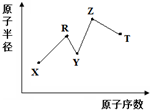 现有短周期主族元素X、Y、Z、R、T,R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族.五种元素原子半径与原子序数之间的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T,R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族.五种元素原子半径与原子序数之间的关系如图所示.下列推断正确的是( )
 现有短周期主族元素X、Y、Z、R、T,R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族.五种元素原子半径与原子序数之间的关系如图所示.下列推断正确的是( )
现有短周期主族元素X、Y、Z、R、T,R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族.五种元素原子半径与原子序数之间的关系如图所示.下列推断正确的是( )| A. | 离子半径:Y<Z | |
| B. | 氢化物的沸点:Y<T | |
| C. | 最高价氧化物对应水化物的酸性:T<R | |
| D. | 由X、Y、Z、R四种元素组成的常见化合物中含有离子键 |