题目内容
2.下列说法错误的是( )| A. | 酒精可以和水以任意比例互溶,与氢键有关 | |
| B. | 邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,与氢键有关 | |
| C. | 无机含氧酸的化学式可以用XOn(OH)m表示,n值越大,m值越小,则该酸的酸性就越强.则可推知,硫酸酸性强于磷酸 | |
| D. | 两分子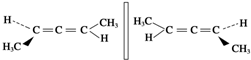 互为手性分子 互为手性分子 |
分析 A、乙醇可以形成氢键,水分子也可以形成氢键,两者之间也可形成氢键,所以可以互溶;
B、邻羟基苯甲醛形成分子内氢键,而对羟基苯甲醛能够形成分子间氢键;
C、据此可知,非羟基氧原子数目越大,酸性越强;
D、根据手性分子是含有手性碳原子的分子;
解答 解:A、乙醇可以形成氢键,水分子也可以形成氢键,两者之间也可形成氢键,所以可以互溶,与氢键有关,故A正确;
B、由于邻羟基苯甲醛形成分子内氢键,使熔沸点偏低;而对羟基苯甲醛能够形成分子间氢键,使熔沸点偏高,所以邻羟基苯甲醛比对羟基苯甲醛熔、沸点低,故B正确;
C、硫酸非羟基氧原子数目是2,而磷酸是1,所以硫酸酸性强于磷酸,故C正确;
D、两分子 中无手性碳,两分子是同一物质,故D错误;
中无手性碳,两分子是同一物质,故D错误;
故选D.
点评 本题考查分子间作用力和分子的极性、手性C原子,根据非羟基氧原子数目多少来确定酸性强弱即可,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列分子中所有碳原子不可能处在同一平面上的是( )
| A. |  | B. |  | C. |  | D. |  |
13.Cu2O是一种半导体材料,基于绿色化学理念设计的一制取Cu2O的电解池示意图如下,电池总反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑.下列说法正确的是( )


| A. | 石墨电极上产生氢气 | |
| B. | 铜电极被还原 | |
| C. | 铜电极接直流电源的负极 | |
| D. | 当有1 mol电子转移时,有1 mol Cu2O生成 |
10.下列说法正确的是( )
| A. | 二氧化碳通入水玻璃可以得到硅酸 | |
| B. | 水泥、玻璃、陶瓷、水晶都属于硅酸盐产品 | |
| C. | 工艺师利用盐酸刻蚀石英制作艺术品 | |
| D. | 可以用澄清石灰水鉴别SO2和CO2 |
17.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图甲).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
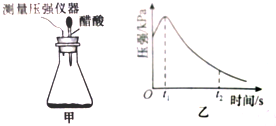 (1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响
(1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响
..
(2)编号①试验测得容器中压强随时间变化如图乙.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧腐蚀,此时,碳粉表面发生了还原(填“氧化”或“还原”)反应,其电极反应式为O2+2H2O+4e-═4OH-.
(3)该小组对图乙中0~t1时压强增大的原因提出了如下假设:
假设一:发生析氢腐蚀产生了气体
假设二:反应开始时放热,导致容器温度升高,压强增大.
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验做参照 | 0.5 | 2.0 | 90.0 |
| ② | 探究醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
 (1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响
(1)上表中编号②实验中铁粉的质量为2.0g;编号③试验的实验目的是探究碳粉的质量对化学反应速率的影响..
(2)编号①试验测得容器中压强随时间变化如图乙.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧腐蚀,此时,碳粉表面发生了还原(填“氧化”或“还原”)反应,其电极反应式为O2+2H2O+4e-═4OH-.
(3)该小组对图乙中0~t1时压强增大的原因提出了如下假设:
假设一:发生析氢腐蚀产生了气体
假设二:反应开始时放热,导致容器温度升高,压强增大.
7.下列化学用语正确的是( )
| A. | 乙烯结构简式为C2H4 | B. | 乙醇的比例模型为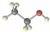 | ||
| C. | 间二甲苯的结构简式为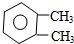 | D. | 甲烷的结构式为 |
14.为了测定某卤代烃分子中所含有的卤原子种类,可按下列步骤进行实验:①量取该卤代烃液体;②冷却后加入稀硝酸酸化;③加入AgNO3溶液至沉淀完全;④加入适量NaOH溶液,煮沸至液体不分层;正确操作顺序为( )
| A. | ④③②① | B. | ①④②③ | C. | ③①④② | D. | ①④③② |
11.某种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水(酸性)中的有机物可用C6H10O5表示[交换膜分别是只允许阴(阳)离子通过的阴(阳)离子交换膜],下列有关说法中不正确的是( )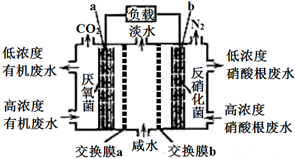

| A. | 电池工作时,电子由a极经导线流向b极 | |
| B. | 交换膜a是阴离子交换膜 | |
| C. | 电极b的反应式:2NO3-+10e-+6H2O=N2↑+12OH- | |
| D. | 相同时间内(相同状况下)生成CO2和N2的体积比为5:2 |