题目内容
17.下列符号中表示电子云伸展方向的是( )| A. | K、L、M、N | B. | s、p、d、f | C. | px、py、pz | D. | ↑、↓ |
分析 S能级电子云的形状为球形,所以电子云无伸展方向,p能级电子云的形状为纺锤形,所以电子云有伸展方向,据此分析.
解答 解:S能级电子云的形状为球形,所以电子云无伸展方向,p能级电子云的形状为纺锤形,所以px、py、pz表示p能级电子云伸展方向,故选:C.
点评 本题考查电子云伸展方向,难度不大,注意S轨道的形状以及p能级的伸展方向即可答题.

练习册系列答案
相关题目
2. 研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:
研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:
(1)生产水煤气过程中有以下反应:
①C(s)+CO2(g)?2CO(g)△H1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3;
若平衡表达式为K=$\frac{c(H_{2})•c(CO)}{c(H_{2}O)}$,则它所对应的化学反应方程式是(填序号)③.
(2)对反应①下列说法中能说明该反应达到平衡状态的bcd
a.温度和体积一定时,混合气体的颜色不再变化
b.温度和体积一定时,容器内的压强不再变化
c.温度和体积一定时,生成物的浓度不再变化
d.温度和体积一定时,混合气体的密度不再变化
(3)不同温度下反应②的平衡常数如下表所示.则△H2<0(填“<”或“>”);在500℃时,把等物质的量浓度的CO和H2O(g)充入反应容器,达到平衡时c(CO)=0.005mol•L-1、c(H2)=0.015mol•L-1,则CO的平衡转化率为75%.
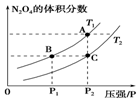
(4)对反应2NO2(g)?N2O4(g)△H<0在温度为T1、T2时,平衡体系N2O4的体积分数随压强变化曲线如图所示.
则T1<T2(填“>”或“<”);增大压强,平衡正反应方向移动(填“正反应方向”或“逆反应方
向”或“不”); B、C两点的平衡常数B>C(填“>”或“<”).
 研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:
研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:(1)生产水煤气过程中有以下反应:
①C(s)+CO2(g)?2CO(g)△H1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3;
若平衡表达式为K=$\frac{c(H_{2})•c(CO)}{c(H_{2}O)}$,则它所对应的化学反应方程式是(填序号)③.
(2)对反应①下列说法中能说明该反应达到平衡状态的bcd
a.温度和体积一定时,混合气体的颜色不再变化
b.温度和体积一定时,容器内的压强不再变化
c.温度和体积一定时,生成物的浓度不再变化
d.温度和体积一定时,混合气体的密度不再变化
(3)不同温度下反应②的平衡常数如下表所示.则△H2<0(填“<”或“>”);在500℃时,把等物质的量浓度的CO和H2O(g)充入反应容器,达到平衡时c(CO)=0.005mol•L-1、c(H2)=0.015mol•L-1,则CO的平衡转化率为75%.
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.945795506 | 9 | 1 |
则T1<T2(填“>”或“<”);增大压强,平衡正反应方向移动(填“正反应方向”或“逆反应方
向”或“不”); B、C两点的平衡常数B>C(填“>”或“<”).
5.将一定量的 SO2(g)和 O2(g)分别通入到体积为 2L 的恒容密闭容器中,在不同温度下进 行反应得到如表中的两组数据:下列说法不正确的是( )
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
| A. | x=1.6 | |
| B. | 实验 1 在前 6min 的反应速率 v(SO2)=0.2mol•L-1•min-1 | |
| C. | T1、T2的关系:T1>T2 | |
| D. | K1、K2的关系:K1>K2 |
12.用中和滴定法确定某烧碱样品的浓度,试根据实验回答下列问题:
(1)准确称取一定量的样品,配成500mL待测溶液.称量时,样品应放在A上称量.
A.小烧杯 B.洁净纸片 C.天平的托盘
(2)试验时用0.2000mol•L-1的盐酸来滴定待测样品溶液,通常不会选用B作指示剂.
A.甲基橙 B.石蕊 C.酚酞
(3)若选用酚酞作指示剂,到达滴定终点的实验现象是当加入最后一滴盐酸时,锥形瓶内溶液刚好由淡红色变为无色且半分钟无颜色变化,这样操作所得实验数据偏小(填“偏大”、“偏小”或“无影响”,下同);若观察酸式滴定管液面时,开始俯视,滴定终点平视,则实验数据偏大.
(4)根据如表数据,计算被测烧碱溶液的物质的量浓度是0.4000mol•L-1.
(1)准确称取一定量的样品,配成500mL待测溶液.称量时,样品应放在A上称量.
A.小烧杯 B.洁净纸片 C.天平的托盘
(2)试验时用0.2000mol•L-1的盐酸来滴定待测样品溶液,通常不会选用B作指示剂.
A.甲基橙 B.石蕊 C.酚酞
(3)若选用酚酞作指示剂,到达滴定终点的实验现象是当加入最后一滴盐酸时,锥形瓶内溶液刚好由淡红色变为无色且半分钟无颜色变化,这样操作所得实验数据偏小(填“偏大”、“偏小”或“无影响”,下同);若观察酸式滴定管液面时,开始俯视,滴定终点平视,则实验数据偏大.
(4)根据如表数据,计算被测烧碱溶液的物质的量浓度是0.4000mol•L-1.
| 滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
| 第一次 | 10.00 | 0.40 | 20.50 |
| 第二次 | 10.00 | 4.10 | 24.00 |
| 第三次 | 10.00 | 0.40 | 21.50 |
 .
.