题目内容
2.下列变化的实质相似的是( )①浓硫酸能在白纸上写字,氢氟酸能在玻璃上刻字
②二氧化硫和氯气均能使品红溶液褪色
③二氧化硫能使高锰酸钾溶液、溴水褪色
④氨气和碘化氢气体均不能用浓硫酸干燥
⑤常温下浓硫酸可用铁容器存放、加热条件下浓硫酸能与木炭反应
⑥浓硫酸和浓盐酸在空气中敞口放置时浓度均减小.
| A. | 只有②③④ | B. | 只有③⑤ | C. | 只有①④⑥ | D. | 全部 |
分析 ①浓硫酸具有强氧化性;氢氟酸具有很强的腐蚀性;
②二氧化硫能和有色物质反应生成无色物质,次氯酸具有强氧化性;
③二氧化硫具有还原性,可与溴水、高锰酸钾发生氧化还原反应;
④氨气显碱性,能与浓硫酸发生化合反应,碘化氢具有还原性,能与浓硫酸发生氧化还原反应;
⑤常温下,浓硫酸能使铁发生钝化,发生的是氧化还原反应,故可用铁的容器存放;在加热条件下浓硫酸能与木炭反应,发生的是氧化还原反应;
⑥浓硫酸具有吸水性,盐酸易挥发.
解答 解:①浓硫酸具有强氧化性,故能在白纸上写字;氢氟酸具有很强的腐蚀性,故能在玻璃上刻字,二者原理不同,故错误;
②二氧化硫能和有色物质反应生成无色物质而体现漂白性,氯气和水反应生成的次氯酸具有强氧化性而体现漂白性,所以二者原理不同,故错误;
③二氧化硫具有还原性,可与溴水、高锰酸钾发生氧化还原反应,原理相同,故正确;
④氨气显碱性,能与浓硫酸发生化合反应,碘化氢具有还原性,能与浓硫酸发生氧化还原反应,原理不同,故错误;
⑤常温下,浓硫酸能使铁发生钝化,发生的是氧化还原反应,故可用铁的容器存放;在加热条件下浓硫酸能与木炭反应,发生的是氧化还原反应,故正确;
⑥浓硫酸具有吸水性,盐酸易挥发,二者放置空气中浓度都变小,但原理不同,故错误;故选B.
点评 本题考查物质之间的反应,明确反应原理是解本题关键,熟悉常见物质的性质,注意二氧化硫、次氯酸漂白原理的差别,二氧化硫不能漂白酸碱指示剂,为易错点.

练习册系列答案
相关题目
10.下列说法正确的是( )
| A. | 高锰酸钾充分加热后的剩余固体、碘酒、空气都是混合物 | |
| B. | Na2O和NH3的水溶液均能导电,故均为电解质 | |
| C. | 氧化还原反应中非金属单质只作氧化剂 | |
| D. | 酸碱中和反应的实质是H+与OH-结合生成水,故酸碱中和反应都可用H++OH-═H2O表示 |
17.下列符号中表示电子云伸展方向的是( )
| A. | K、L、M、N | B. | s、p、d、f | C. | px、py、pz | D. | ↑、↓ |
7.互为同分异构体,且可用银镜反应区别的是( )
| A. | 丙酸和乙酸甲酯 | B. | 蔗糖和麦芽糖 | C. | 麦芽糖和纤维素 | D. | 苯甲酸和苯甲醛 |
11.下列金属的冶炼原理中,属于热分解法的是( )
| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2↑ | ||
| C. | Fe+CuSO4═FeSO4+Cu | D. | 2NaCl(熔融)$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2↑ |
12.A2、B2、C2三种单质和它们离子间能发生下列反应:
①2A-+C2═2C-+A2
②2C-+B2═2B-+C2
则有关说法中不正确的是( )
①2A-+C2═2C-+A2
②2C-+B2═2B-+C2
则有关说法中不正确的是( )
| A. | 氧化性:B2>C2>A2 | |
| B. | 在含有C-和A-的溶液中加入B2,C-优先发生反应 | |
| C. | 还原性:A->C->B- | |
| D. | 在含有B2和C2的溶液中加入A-,B2优先发生反应 |
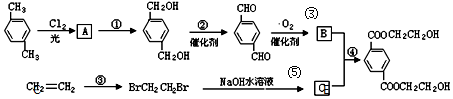
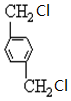 、B、
、B、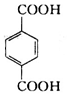 、C.HOCH2CH2OH、
、C.HOCH2CH2OH、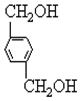 +2NaCl;
+2NaCl; ,反应的化学方程式是
,反应的化学方程式是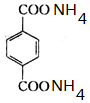 +2H2O.
+2H2O.