题目内容
10.某反应物浓度在5min中内浓度由8mol/L 减少了3mol/L,它的化学反应速率是多少?分析 反应物浓度在5min中内浓度由8mol/L 减少了3mol/L,带入v=$\frac{△c}{△t}$计算;
解答 解:反应物浓度在5min中内浓度由8mol/L 减少了3mol/L,v=$\frac{3mol/L}{5min}$=0.6mol/L•min,
答:某反应物浓度在5min中内浓度由8mol/L 减少了3mol/L,它的化学反应速率为0.6mol/L•min;
点评 本题考查了化学反应速率的计算,难度不大,学习中注意化学反应速率概念的理解应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20. 据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的水合物(CH4•nH2O).
据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的水合物(CH4•nH2O).
(1)在常温常压下,“可燃冰”会发生分解反应,其化学方程式是CH4•nH2O=CH4↑+nH2O.
(2)甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油.
①在101KPa时,1.6g CH4(g)与H2O(g)反应生成CO、H2,吸热20.64kJ.则甲烷与H2O(g)反应的热化学方程式:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.4 kJ•mol-1.
②CH4不完全燃烧也可制得合成气:CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g);
△H=-35.4kJ•mol-1.则从原料选择和能源利用角度,比较方法①和②,合成甲醇的适宜方法为②(填序号);原因是选择CH4不完全燃烧,制合成气体时,放出热量,同时得到CO:H2为1:2,能恰好完全反应合成甲醇.
(3)利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)=CH3OH(g)△H1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)=CO(g)+H2O(g)△H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
由此计算△H1=-99kJ•mol-1,已知△H2=-58kJ•mol-1,则△H3=+41kJ•mol-1.
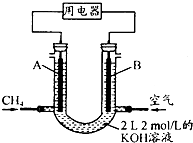
(4)可燃冰中CH4的其它用途是,将CH4设计成燃料电池,其利用率更高,装置示意图(A、B为多孔性碳棒).持续通人甲烷,在标准状况下,消耗甲烷体积VL.
①O<V≤44.8L时,电池总反应方程式为CH4+2O2+2KOH=K2CO3+3H2O,
②44.8L<V≤89.6L时,负极电极反应为CH4-8e-+9CO32-+3H2O=10HCO3-.
 据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的水合物(CH4•nH2O).
据报道,在西藏冻土的一定深度下,发现了储量巨大的“可燃冰”,它主要是甲烷和水形成的水合物(CH4•nH2O).(1)在常温常压下,“可燃冰”会发生分解反应,其化学方程式是CH4•nH2O=CH4↑+nH2O.
(2)甲烷可制成合成气(CO、H2),再制成甲醇,代替日益供应紧张的燃油.
①在101KPa时,1.6g CH4(g)与H2O(g)反应生成CO、H2,吸热20.64kJ.则甲烷与H2O(g)反应的热化学方程式:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.4 kJ•mol-1.
②CH4不完全燃烧也可制得合成气:CH4(g)+$\frac{1}{2}$O2(g)═CO(g)+2H2(g);
△H=-35.4kJ•mol-1.则从原料选择和能源利用角度,比较方法①和②,合成甲醇的适宜方法为②(填序号);原因是选择CH4不完全燃烧,制合成气体时,放出热量,同时得到CO:H2为1:2,能恰好完全反应合成甲醇.
(3)利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g)=CH3OH(g)△H1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H2
③CO2(g)+H2(g)=CO(g)+H2O(g)△H3
回答下列问题:
已知反应①中相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 1 076 | 465 | 413 |
(4)可燃冰中CH4的其它用途是,将CH4设计成燃料电池,其利用率更高,装置示意图(A、B为多孔性碳棒).持续通人甲烷,在标准状况下,消耗甲烷体积VL.
①O<V≤44.8L时,电池总反应方程式为CH4+2O2+2KOH=K2CO3+3H2O,
②44.8L<V≤89.6L时,负极电极反应为CH4-8e-+9CO32-+3H2O=10HCO3-.
15.下列选项的化合物中,在常温、常压下以液态形式存在的是( )
| A. | 丙烷 | B. | 乙炔 | C. | 乙烯 | D. | 乙醇 |
2.下列物质属于烃的含氧衍生物的是( )
| A. | CHCl3 | B. | CCl4 | C. | 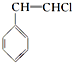 | D. | 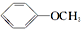 |
19.下列化学反应△H最小的是( )
| A. | NaOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l);△H1 | |
| B. | NaOH(aq)+$\frac{1}{2}$H2SO4(浓)═$\frac{1}{2}$Na2SO4(aq)+H2O(l);△H4 | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq )+H2O(l);△H2 | |
| D. | CH3COOH(aq)+NaOH(aq)═CH3COONa (aq )+H2O(l);△H3 |
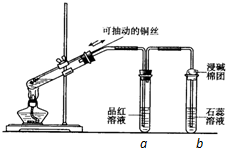 某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中.请回答下列问题:
某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中.请回答下列问题:
 形成六元环酯的结构简式
形成六元环酯的结构简式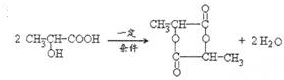 .
.