题目内容
1.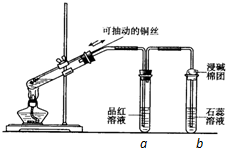 某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中.请回答下列问题:
某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中.请回答下列问题:(1)写出铜与浓硫酸反应的化学方程式Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)试管a、b分别检验生成气体的性质,写出观察到的现象及其作用.
试管a中的现象是放出的气体能使品红溶液褪色,作用是证明二氧化硫有漂白性.
试管b中的现象是放出的气体使紫色石蕊溶液变红,作用是证明二氧化硫有酸性.
(3)如图将铜丝改为可抽动的铜丝符合化学实验“绿色化”的原因是通过调节铜丝的高度,可以控制参加反应的铜与浓硫酸的接触面积),从而控制SO2产生的量,减少SO2的污染..
分析 (1)铜与浓硫酸加热反应生成硫酸铜、二氧化硫和水;
(2)依据二氧化硫的漂白性和酸性解答;
(3)通过调节铜丝的高度,可以控制反应的开始与结束,减少了污染气体的排放、节约了原料.
解答 解:(1)铜与浓硫酸加热反应生成硫酸铜、二氧化硫和水,方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O;
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O;
(2)二氧化硫能够与有色物质化合生成无色物质,具有漂白性,能够使品红溶液褪色;二氧化硫为酸性氧化物,能够与水反应生成亚硫酸,亚硫酸电离产生氢离子,溶液具有酸性,遇到石蕊显红色;
故答案为:放出的气体能使品红溶液褪色;证明二氧化硫有漂白性;放出的气体使紫色石蕊溶液变红;证明二氧化硫有酸性;
(3)将铜丝改为可抽动的铜丝后,通过调节铜丝的高度,可以可知参加反应的铜与浓硫酸的接触面积,从而可知二氧化硫产生的量,减少二氧化硫的污染,该方法符合绿色化学的理念,
故答案为:通过调节铜丝的高度,可以可知参加反应的铜与浓硫酸的接触面积,从而可知二氧化硫产生的量,减少二氧化硫的污染.
点评 本题考查了浓硫酸的性质、二氧化硫的性质及检验,注意掌握铜与浓硫酸反应原理、二氧化硫气体的性质及检验方法,明确性质实验方案设计与评价的原则,题目难度中等.

练习册系列答案
相关题目
11.分子式为C5H10O2的有机物能与NaHCO3反应放出气体的结构有多少种( )
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
16.下列有关元素周期表的说法不正确的是( )
| A. | 第15列某元素能形成碱性气体 | |
| B. | 第2列元素中肯定没有非金属元素 | |
| C. | 第17列的第一种元素的原子序数为8 | |
| D. | 短周期中能与强碱反应产生H2的金属元素位于第ⅢA族 |
6.下列有机物的命名正确的是( )
| A. | 二溴乙烷: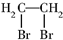 | B. | 3-乙基-1-丁烷: | ||
| C. | 2,2,3-三甲基戊烷: | D. | 2-甲基-2,4-己二烯: |
13.X、Y、Z 均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-离子具有相同的电子层结构.下列说法正确的是( )
| A. | 原子半径:X>Y>Z | B. | 单质沸点:X>Y>Z | ||
| C. | 原子最外层电子数:X>Y>Z | D. | 原子序数:X>Y>Z |
11.有关原子最外层电子排布为(n+1)sn(n+1)p n+1的元素及其化合物,下列叙述中不正确的是( )
| A. | 氢化物受热易分解 | |
| B. | 该元素是植物生长所需要的一种营养元素 | |
| C. | 其单质既有氧化性又有还原性 | |
| D. | 最高价氧化物对应的水化物是一种强酸 |
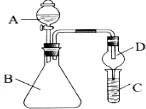 利用如图装置可验证同主族元素非金属性的变化规律
利用如图装置可验证同主族元素非金属性的变化规律