题目内容
11.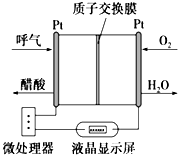 如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.其中电极均为Pt电极.下列说法不正确的是( )
如图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测.其中电极均为Pt电极.下列说法不正确的是( )| A. | 电流由O2所在的铂电极经外电路流向另一电极 | |
| B. | O2在右侧电极发生还原反应,且该电极附近溶液的pH升高 | |
| C. | 该电池的负极反应式为:CH3CH2OH+3H2O-12e-═2CO2↑+12H+ | |
| D. | 微处理器通过检测电流大小而计算出被测气体中酒精的含量 |
分析 该装置中含有质子交换膜,则电解质溶液为酸性,酸性条件下,乙醇燃料电池中,负极上乙醇失电子发生氧化反应,正极上是氧气得电子的还原反应;根据图示得出酸性燃料电池的反应物和生成物,再根据原电池原理写出该电池的反应式来判断.
解答 解:A.乙醇燃料电池中,负极上乙醇失电子发生氧化反应,正极上是氧气得电子的还原反应,电流由正极流向负极,即从O2所在的铂电极经外电路流向另一电极,故A正确;
B.燃料电池中,正极上是氧气得电子的还原反应,O2所在的铂电极处发生还原反应,电极反应为O2+4e-+4H+═2H2O,氢离子被消耗,酸性减弱,PH值升高,故B正确;
C.该电池的负极上乙醇失电子发生氧化反应,由装置图可知酒精在负极被氧气氧化发生氧化反应生成醋酸,CH3CH2OH-4e-+H2O=4H++CH3COOH,故C错误;
D.根据微处理器通过检测电流大小可以得出电子转移的物质的量,根据电极反应式可以计算出被测气体中酒精的含量,故D正确;
故选:C.
点评 本题以乙醇为燃料考查了燃料电池,难度不大,注意正负极上电极反应式的书写要结合电解质溶液的酸碱性,即使燃料和氧化剂相同,如果电解质溶液不同,电极反应式也不同.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
19.在水中加入下列物质,可使水的电离平衡正向移动,且所得溶液呈酸性的是( )
| A. | NaCl | B. | H2SO4 | C. | Na2CO3 | D. | NH4Cl |
16.在pH=1的无色溶液中,下列各离子组因发生氧化还原反应而不能共存的是( )
| A. | NH4+ K+ Na+ CO32- NO3- | B. | K+ Na+ Fe2+ SO42- NO3- | ||
| C. | NH4+ K+ Na+ HCO3-Cl- | D. | NH4+ K+ Na+ NO3- I- |
3.A、B、C、D都是短周期元素,原子半径:D>C>A>B.已知A、B处在同一周期,A、C处在同一主族,C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层上的电子数是D原子最外层电子数的3倍.下列说法中正确的是( )
| A. | 简单离子半径:D>B | |
| B. | 气态氢化物的稳定性:A>B | |
| C. | B、D两元素可组成阴、阳离子个数比为1:1的化合物 | |
| D. | B、C、D三种元素可组成化学式为DCB2的化合物,其水溶液显碱性 |
20.早在古代,我国人民就积累了不少对化学物质变化的认识.例如,晋代炼丹家、医学家葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银,积变又成丹砂”.这句话中的丹砂指的是HgS,下列关于这句话的说法正确的是( )
| A. | 这个过程只涉及物理变化 | |
| B. | 这个过程是可逆反应 | |
| C. | 这个过程发生了复分解反应 | |
| D. | “丹砂烧之成水银”过程中还可能产生SO2 |
 .
.
 .
.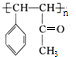 .
.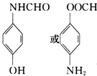 .
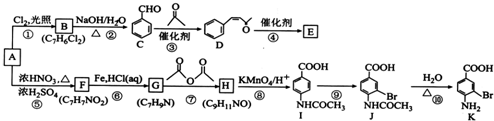
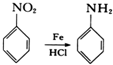
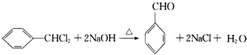
.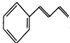 的合成路线补充完整.
的合成路线补充完整.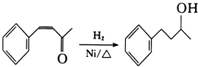 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$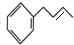 $\stackrel{Br_{2}}{→}$
$\stackrel{Br_{2}}{→}$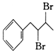 $→_{△}^{NaOH醇溶液}$
$→_{△}^{NaOH醇溶液}$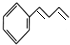 (无机试剂及溶剂任选).
(无机试剂及溶剂任选).