题目内容
4.下列反应中一定属于吸热反应的是( )| A. | 需加热或点燃才能引发的反应 | |
| B. | 氧化还原反应 | |
| C. | 氢氧化钡晶体和氯化铵晶体混合搅拌 | |
| D. | 一氧化碳和氧气反应 |
分析 常见的放热反应有:所有的物质燃烧、所有金属与酸或与水、所有中和反应、绝大多数化合反应、铝热反应;
常见的吸热反应有:绝大数分解反应、个别的化合反应(如C和CO2)、工业制水煤气、碳(一氧化碳、氢气)还原金属氧化物、某些复分解(如铵盐和强碱).
解答 解:A.燃烧反应需要加热或点燃引发,但是燃烧属于放热反应,故A错误;
B.氧化还原不一定属于放热反应,故B错误;
C.氢氧化钡与氯化铵反应属于吸热反应,故C正确;
D.一氧化碳与氧气反应属于燃烧,是放热反应,故D错误,故选C.
点评 本题考查化学反应中能量变化,题目难度不大,掌握常见的放热反应和吸热反应是解题的关键.

练习册系列答案
 全优测试卷系列答案
全优测试卷系列答案 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
14.已知:(1)某无机高分子混凝剂的化学式可表示为Al2(OH)nClm•yH2O; (2)AgF+Cl2+H2O→AgCl+AgClO3+HF+O2(未配平).则( )
| A. | 混凝剂具有强氧化性 | |
| B. | Al2(OH)nClm•yH2O化学式中m等于3-n | |
| C. | 若(2)中Cl2化学计量数为a,则AgF的化学计量数为3a | |
| D. | 若(2)中AgClO3、O2的化学计量数分别为b、c,则AgCl的化学计量数为5b+4c |
15.下列试剂不能用于区分SO2和CO2的是( )
| A. | 澄清石灰水 | B. | 酸性高锰酸钾溶液- | ||
| C. | 溴水 | D. | 硝酸钡溶液 |
19.下列反应的离子方程式书写正确的是( )
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向Al2(SO4)3溶液中加入过量NH3?H2O:Al3++4NH3?H2O═AlO2-+4NH4++2H2O | |
| C. | 酸性溶液中KClO3与KCl反应生成Cl2:ClO3-+Cl-+6H+═Cl2↑+3H2O | |
| D. | 向含1molNaHSO3的溶液中加入1molNa2O2:Na2O2+HSO3-═2Na++SO42-+OH- |
9.将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g)+Y(g)═2Z(g)△H<0.当改变某个条件并达到新平衡后,下列叙述正确的是( )
| A. | 升高温度,X的物质的量减小 | |
| B. | 增大压强(缩小容器体积),Z的浓度不变 | |
| C. | 保持容器体积不变,充入一定量的惰性气体,Y的浓度不变 | |
| D. | 保持容器体积不变,充入一定量的Z,重新平衡时,Y的体积分数增大 |
16.如图是某同学设计的验证原电池和电解池的实验装置,下列说法不正确的是( )
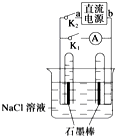

| A. | 若关闭K2、打开K1,一段时间后,发现左侧试管收集到的气体比右侧略多,则a为正极,b为负极 | |
| B. | 关闭K2,打开K1,一段时间后,用拇指堵住试管移出烧 杯,向试管内滴入酚酞,发现左侧试管内溶液变红色,则 a为负极,b为正极 | |
| C. | 若直流电源a为负极,b为正极,关闭K2,打开K1,一段时间后,再关闭K1,打开K2,则电路中电流方向为从右侧石墨棒沿导线到左侧石墨棒 | |
| D. | 若直流电源a为负极,b为正极,关闭K2,打开K1,一段时间后,再关闭K1,打开K2,则左侧石墨棒上发生的电极反应为H2-2e-+2OH-═2H2O |
13.下列有关“化学与生活”描述不正确的是( )
| A. | 核能的利用可能会造成放射性污染,应该立即关闭所有核电站 | |
| B. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| C. | 泡沫灭火器中使用了盐类水解的原理 | |
| D. | 宁德新能源公司生产的锂离子电池可以将化学能转化为电能 |
14.下列无色透明水溶液中,能大量共存的一组离子是( )
| A. | K+、Mg2+、CO32-、Cl- | B. | Na+、Ba2+、HCO3-、OH- | ||
| C. | Mg2+、H+、Cl-、SO42- | D. | K+、SO42-、Cu2+、NO3- |