��Ŀ����
10���Լױ�Ϊԭ�������㶹��������ͼ��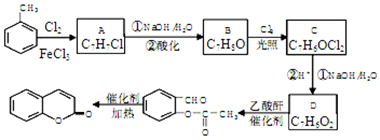
��֪��
��i�� B��FeCl3��Һ������ɫ��Ӧ��
��ii��ͬһ��̼ԭ�����������ǻ�ͨ�����ȶ�������ˮ�γ��ʻ���
��1��A��������2-�ȼױ���C�Ľṹ��ʽ��
 ��A��B�ķ�Ӧ������ȡ����Ӧ��
��A��B�ķ�Ӧ������ȡ����Ӧ����2��D�к��еĹ�����������ȩ�����ǻ���D����������
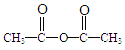 ����Ӧ��������
����Ӧ�������� 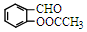 �⣬ͬʱ���ɵ���һ�ֲ���Ľṹ��ʽ��CH3COOH��
�⣬ͬʱ���ɵ���һ�ֲ���Ľṹ��ʽ��CH3COOH����3����
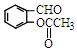 ��Ϊͬ���칹�壬�Ҿ��������ص㣺
��Ϊͬ���칹�壬�Ҿ��������ص㣺��a�����б�����b���ܷ���������Ӧ��c����NaHCO3��Һ��Ӧ�ɷų������������������ͬ���칹�干��17�֣�
���� �ױ����������Ȼ������������·���������ȡ����Ӧ����A��A����±������ˮ�ⷴӦ�õ�B��B�ڹ�����������������������ȡ����Ӧ����C��C�ڷ���±����ˮ�ⷴӦ���ữ�õ�D��D�к���-CHO�����ǻ���D����������Ӧ���� ������ȡ����Ӧ�����������ᣬ��֪DΪ
������ȡ����Ӧ�����������ᣬ��֪DΪ ����CΪ
����CΪ ��BΪ
��BΪ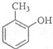 ��AΪ
��AΪ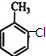 ��
��
��� �⣺�ױ����������Ȼ������������·���������ȡ����Ӧ����A��A����±������ˮ�ⷴӦ�õ�B��B�ڹ�����������������������ȡ����Ӧ����C��C�ڷ���±����ˮ�ⷴӦ���ữ�õ�D��D�к���-CHO�����ǻ���D����������Ӧ���� ������ȡ����Ӧ�����������ᣬ��֪DΪ
������ȡ����Ӧ�����������ᣬ��֪DΪ ����CΪ
����CΪ ��BΪ
��BΪ ��AΪ
��AΪ ��
��
��1��AΪ ��������2-�ȼױ���C�Ľṹ��ʽ��
��������2-�ȼױ���C�Ľṹ��ʽ�� ��A��B�ķ�Ӧ�����ǣ�ȡ����Ӧ��
��A��B�ķ�Ӧ�����ǣ�ȡ����Ӧ��
�ʴ�Ϊ��2-�ȼױ��� ��ȡ����Ӧ��
��ȡ����Ӧ��
��2��DΪ �����еĹ����������ǣ�ȩ�����ǻ���D����������
�����еĹ����������ǣ�ȩ�����ǻ���D���������� ����Ӧ��������
����Ӧ�������� �⣬ͬʱ���ɵ���һ�ֲ���Ľṹ��ʽ�ǣ�CH3COOH��
�⣬ͬʱ���ɵ���һ�ֲ���Ľṹ��ʽ�ǣ�CH3COOH��
�ʴ�Ϊ��ȩ�����ǻ���CH3COOH��
��3���� ��Ϊͬ���칹�壬�Ҿ��������ص㣺��a�����б��� ��b���ܷ���������Ӧ��˵������ȩ������c����NaHCO3��Һ��Ӧ�ɷų����壬˵������-COOH������һ������Ϊ-CH��CHO��COOH�����Ժ���2������Ϊ-CH2COOH��-CHO������-CH2CHO��-COOH�������ڡ��䡢��3�֣����Ժ���3������Ϊ-CH3��-COOH��-CHO����-CH3��-COOH������λʱ��-CHO��4��λ�ã���-CH3��-COOH���ڼ�λʱ��-CHO��4��λ�ã�
��Ϊͬ���칹�壬�Ҿ��������ص㣺��a�����б��� ��b���ܷ���������Ӧ��˵������ȩ������c����NaHCO3��Һ��Ӧ�ɷų����壬˵������-COOH������һ������Ϊ-CH��CHO��COOH�����Ժ���2������Ϊ-CH2COOH��-CHO������-CH2CHO��-COOH�������ڡ��䡢��3�֣����Ժ���3������Ϊ-CH3��-COOH��-CHO����-CH3��-COOH������λʱ��-CHO��4��λ�ã���-CH3��-COOH���ڼ�λʱ��-CHO��4��λ�ã�
��-CH3��-COOH���ڶ�λʱ��-CHO��2��λ�ã��ʷ���������ͬ���칹�干��17�֣�
�ʴ�Ϊ��17��
���� ���⿼���л����ƶϣ�Ϊ�߿���Ƶ�㣬��B������Ϊͻ�ƿڲ��������ϵķ��������ƶϣ�ע���Ϸ�Ӧ�����������Ϣ������ע���л���ɼ��Ͷϼ���ʽ���ѵ���ͬ���칹��������жϣ���Ŀ�Ѷ��еȣ�

 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�| ѡ�� | �� | �� |
| A | Ba��OH��2��Һ�����NaHCO3��Һ��� | NaOH��Һ�����NaHCO3��Һ��� |
| B | ����CO2ͨ��Ba��OH��2��Һ�� | ����CO2ͨ��Ba��OH��2��Һ�� |
| C | BaCl2��Һ��Na2CO3��Һ��� | Ba��OH��2��Һ��NaHCO3��Һ��� |
| D | ����NaHCO3��Һ�������ʯ��ˮ�� | ����NaOH��Һ����Ca��HCO3��2��Һ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
��1���ڹ̶�������ܱ������У��������»�ѧ��Ӧ��N2��g��+3H2��g��2NH3��g������H��0����ƽ�ⳣ��K���¶�T�Ĺ�ϵ�����
| T/K | 298 | 398 | 498 |
| ƽ�ⳣ��K | 4.1��106 | K1 | K2 |
a��������N2��H2��NH3��Ũ��֮��Ϊ1��3��2b��v��N2��=3v��H2��c��������ѹǿ���ֲ���d�����������ܶȱ��ֲ���
��2��������N2H4�������������ȼ��ʱ����������N2O4��Ӧ����N2��ˮ������ijͬѧ�����һ��N2H4--��������ȼ�ϵ�أ����øõ�ص��100mL-��Ũ��NaCl��CuSO4�����Һ����װ����ͼ��ʾ��
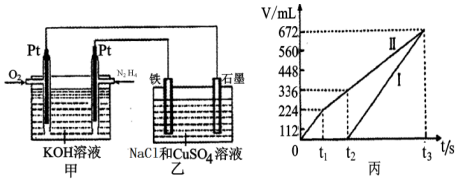
�ٸ�ȼ�ϵ�صĸ�����ӦʽΪ��N2H4+4OH--4e-=N2��+4H2O��������������������������������ʱ��仯�Ĺ�ϵ���ͼ��ʾ����������ѻ���ɱ�״���µ��������ԭ�����Һ��NaCl�����ʵ���Ũ��Ϊ0.2mol/L������t2ʱ������Һ��pHΪ0.7����������Һ������䣬����һλС����lg2=0.3��
| A�� | Xԭ������������Ϊ5 | |
| B�� | ����3mol X2����ʱ��ת��5mol���� | |
| C�� | ��������ͻ�ԭ��������ʵ���֮��Ϊ5��1 | |
| D�� | �������������������������ΪX- |
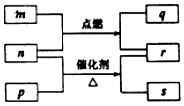 ������Ԫ��W��X��Y��Z��ԭ��������������m��p��q��r��s������ЩԪ����ɵĶ�Ԫ��������³�ѹ��r ΪҺ�壬�����Ϊ��ɫ���壬m��Ħ������Ϊp��2����n��Ԫ��Y�ĵ��ʣ�q��ʹƷ����Һ��ɫ��������ת����ϵ��ͼ��ʾ������˵���в���ȷ���ǣ�������
������Ԫ��W��X��Y��Z��ԭ��������������m��p��q��r��s������ЩԪ����ɵĶ�Ԫ��������³�ѹ��r ΪҺ�壬�����Ϊ��ɫ���壬m��Ħ������Ϊp��2����n��Ԫ��Y�ĵ��ʣ�q��ʹƷ����Һ��ɫ��������ת����ϵ��ͼ��ʾ������˵���в���ȷ���ǣ�������| A�� | ԭ�Ӱ뾶��Y��X��Z | B�� | �ǽ����ԣ�Y��X��W | ||
| C�� | m��q��n��s�����ܹ��� | D�� | ��n������q�����Լ���ȼ�� |
| A�� | ������̼�ᱵ��Ӧ CO32-+2H+�TCO2��+H2O | |
| B�� | ����ͭ��Һ�еμ�����������Һ Ba2++2OH-+Cu2++SO42-�TBaSO4��+Cu��OH��2�� | |
| C�� | ��������Һ�м���ͭ�� Ag++Cu�TCu2++Ag�� | |
| D�� | ����ϡ���ᷴӦ 2Fe+6H+�T2Fe3++3H2�� |
| ��� | �Ȼ�ѧ����ʽ | ��ѧƽ�ⳣ�� |
| �� | CO��g��+2H2��g��?CH3OH��g����H1=-99kJ•mol-1 | K1 |
| �� | 2CH3OH��g��?CH3OCH3��g��+H2O��g����H2=-24kJ•mol-1 | K2 |
| �� | CO��g��+H2O��g��?CO2��g��+H2��g����H3=-41kJ•mol-1 | K3 |
��1���ù��յ��ܷ�ӦΪ3CO��g��+3H2��g��?CH3OCH3��g��+CO2��g����H���÷�Ӧ��H=-263 kJ•mol-1����ѧƽ�ⳣ��K=K12•K2•K3���ú�K1��K2��K3�Ĵ���ʽ��ʾ����
��2�����д�ʩ�У������CH3OCH3���ʵ���AD��
A������������� B�������¶�
C�����ø�Ч���� D������ѹǿ
��3�������з�Ӧ�ٺͷ�Ӧ�ڷֱ��ڲ�ͬ�ķ�Ӧ���н��У���Ӧ�۷������ù����з�Ӧ�۵ķ��������CH3OCH3�IJ��ʣ�ԭ���Ƿ�Ӧ�������˷�Ӧ���еIJ���H2O��ʹ��Ӧ�ڵĻ�ѧƽ��������Ӧ�����ƶ����Ӷ����CH3OCH3�IJ��ʣ�
��4����n��H2��/n��CO��=2 ͨ��1L�ķ�Ӧ���У�һ�������·�����Ӧ��4H2��g��+2CO��g��?CH3OCH3��g��+H2O��g����H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ��ʾ������˵����ȷ����CD��
A���÷�Ӧ�ġ�H��0
B������p2��316��ʱ��Ӧ�ﵽƽ�⣬��CO��ת����С��50%
C������p3��316��ʱ��Ӧ�ﵽƽ�⣬H2��ת���ʵ���50%
D������p3��316��ʱ����ʼʱn��H2��/n��CO��=3�����ƽ��ʱCO��ת���ʴ���50%

��5��ij�¶��£���8.0mol H2��4.0mol CO�����ݻ�Ϊ2L���ܱ������У�������Ӧ��4H2��g��+2CO��g��?CH3OCH3��g��+H2O��g������Ӧ��ƽ����ö����ѵ��������Ϊ25%������¶��·�Ӧ��ƽ�ⳣ��K=2.25��
| A�� | KCl���� | B�� | Zn�� | C�� | SO3���� | D�� | CuSO4���� |

 $\stackrel{2R��OH}{��}$2ROH+
$\stackrel{2R��OH}{��}$2ROH+
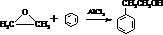 ��
��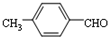 ��
�� ��
�� �ĺϳ�·�ߣ����һ����2-�ȱ���ͱ�Ҫ�����Լ��Ʊ�
�ĺϳ�·�ߣ����һ����2-�ȱ���ͱ�Ҫ�����Լ��Ʊ� �ĺϳ�·�ߣ���ע����Ҫ�ķ�Ӧ������
�ĺϳ�·�ߣ���ע����Ҫ�ķ�Ӧ������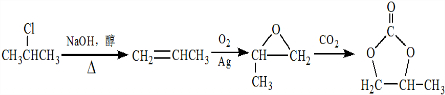 ��
��