题目内容
20.设NA表示阿伏加德罗常数,下列说法中正确的是( )| A. | 标准状况下,22.4LSO3所含的分子数为NA | |
| B. | 49g硫酸中所含氧原子的数目为2NA | |
| C. | 1molNH4+所含质子数为10NA | |
| D. | 0.5L 0.2 mol•L-1硫酸钠溶液中含有的SO42-离子数目为0.2NA |
分析 A.气体摩尔体积使用对象为气体;
B.依据n=$\frac{m}{M}$计算硫酸的物质的量结合硫酸分子构成解答;
C.1个铵根离子含有11个质子;
D.依据n=CV计算硫酸钠的物质的量,1mol硫酸含有1mol硫酸根离子,据此解答;
解答 解:A.标况下三氧化硫不是气体,不能使用气体摩尔体积,故A错误;
B.1个硫酸分子含有4个O,49g硫酸物质的量为:$\frac{49g}{98g/mol}$=0.5mol,所含氧原子的数目为0.5mol×4×NA=2NA,故B正确;
C.1molNH4+所含质子数为11NA,故C错误;
D.0.5L 0.2 mol•L-1硫酸钠溶液中含有硫酸钠的物质的量为.5L×0.2 mol•L-1=0.1mol,含有的SO42-离子数目为0.1NA,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是阿伏伽德罗常数的规定和计算判断,明确以物质的量为核心的计算公式,熟悉物质的结构与组成是解题关键,注意气体摩尔体积使用条件和对象,题目难度不大.

练习册系列答案
相关题目
17.25℃时,在等体积的下列溶液中,发生电离的水的物质的量之比是( )
①0.5mol•L-1的H2SO4溶液,②0.05mol•L-1的Ba(OH)2溶液,③1mol•L-1的NaCl溶液,④纯水.
①0.5mol•L-1的H2SO4溶液,②0.05mol•L-1的Ba(OH)2溶液,③1mol•L-1的NaCl溶液,④纯水.
| A. | 107:107:1:1 | B. | 1:10:107:107 | C. | 107:106:2:2 | D. | 107:106:2×107:2 |
11.如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )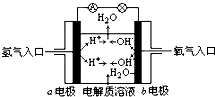

| A. | b电极是负极 | |
| B. | 总反应方程式为:2H2+O2═2H2O | |
| C. | 负极发生还原反应,正极发生氧化反应 | |
| D. | 氢氧燃料电池是一种具有广泛应用前景的绿色电源 |
8.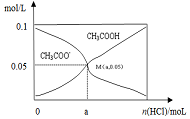 常温下向10mL 0.1mol•L-1CH3COONa溶液中,不断通入HCl后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液体积变化),下列说法不正确的是( )
常温下向10mL 0.1mol•L-1CH3COONa溶液中,不断通入HCl后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液体积变化),下列说法不正确的是( )
 常温下向10mL 0.1mol•L-1CH3COONa溶液中,不断通入HCl后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液体积变化),下列说法不正确的是( )
常温下向10mL 0.1mol•L-1CH3COONa溶液中,不断通入HCl后,CH3COO-与CH3COOH浓度的变化趋势如图所示(不考虑溶液体积变化),下列说法不正确的是( )| A. | M点溶液中水的电离程度比原溶液小 | |
| B. | 在M点时,c(H+)-c(OH-)=(100a-5.0×10-2) mol/L | |
| C. | 随着HCl的通入,$\frac{c(O{H}^{-})}{c(C{H}_{2}CO{O}^{-})}$值不断减小 | |
| D. | 当n(HCl)=1.0×10-3mol时,溶液中c(Na+)>c(Cl-)>c(CHCOO-)>c(H+)>c(OH-) |
15. 某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:
某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:
A.移取20.00mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至0刻度以上 2~3cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成下列问题:
(1)正确操作步骤的顺序是B、D、C、E、A、F(填字母序号).
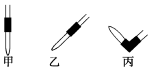
(2)如图,排除碱式滴定管中气泡的方法应采用操作丙(填图编号),轻轻挤压玻璃球使尖嘴部分充满碱液.
(3)上述B步骤操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差.
(4)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则滴定结果偏高(填“偏高”、“偏低”或“不变”).
(5)判断到达滴定终点的实验现象是滴入最后一滴KOH溶液,溶液由无色变为浅红色,且在半分钟内不褪色.
(6)重复上述滴定2~3次,记录数据如表:
根据表中数据,可计算出该盐酸的浓度约为0.09mol/L(保留两位小数).
 某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:
某学生用0.100mol•L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:A.移取20.00mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至0刻度以上 2~3cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度.
就此实验完成下列问题:
(1)正确操作步骤的顺序是B、D、C、E、A、F(填字母序号).
(2)如图,排除碱式滴定管中气泡的方法应采用操作丙(填图编号),轻轻挤压玻璃球使尖嘴部分充满碱液.
(3)上述B步骤操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差.
(4)上述A步骤操作之前,若先用待测溶液润洗锥形瓶,则滴定结果偏高(填“偏高”、“偏低”或“不变”).
(5)判断到达滴定终点的实验现象是滴入最后一滴KOH溶液,溶液由无色变为浅红色,且在半分钟内不褪色.
(6)重复上述滴定2~3次,记录数据如表:
| 实验 编号 | KOH溶液的浓度(mol•L-1) | 滴定完成时,滴入KOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
5.下列关于物质的量的叙述中,正确的是( )
| A. | 1 mol任何物质中都含有6.02×1023个分子 | |
| B. | 0.012 kg 12C中含有约6.02×1023 NA个碳原子 | |
| C. | 1 mol水中含有1 mol氢分子和1 mol氧原子 | |
| D. | 1 mol Ne中约含有6.02×1024个电子 |
12.下列反应中,不属于氧化还原反应的是( )
| A. | H2+F2═2HF | B. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 | ||
| C. | NaOH+HCl═NaCl+H2O | D. | 4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$ 2H2O+4NO2↑+O2↑ |
9.用NA表示阿伏加德罗常数,下列有关说法正确的是( )
| A. | 71 g Cl2所含原子数为2NA | |
| B. | 在常温常压下,1 mol氦气含有的原子数为2NA | |
| C. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA | |
| D. | 标准状况下,1 mol H2O和1 mol H2的体积都约为22.4 L |
10.下列反应中,观察不到颜色变化的是( )
| A. | 往氨水中滴加酚酞 | B. | NO气体暴露在空气中 | ||
| C. | Cl2通过湿润的有色布条 | D. | 往NaOH溶液中通入CO2 |