题目内容
 I.下列有关实验的说法不正确的是
I.下列有关实验的说法不正确的是(A)实验室制乙烯时,温度计水银球应插入混合液中,而石油分馏时则不能插入混合液中.
(B)配制氢氧化铜悬浊液时,向硫酸铜溶液中逐滴滴加氢氧化钠溶液,直到沉淀完全为止.
(C)配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止.
(D)用醋酸、碳酸氢钠、苯酚钠和必须的仪器可以检验苯酚、醋酸、碳酸的酸性强弱.
(E)做过银镜反应的试管用浓硝酸清洗.
(F)卤代烃与氢氧化钠溶液共热后,再滴入硝酸银溶液,可检验卤原子的种类.
(G) 若苯酚不慎沾到皮肤上,应立即用酒精洗涤.
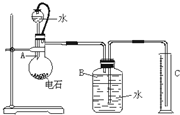
II.现欲在室温和大气压强下,用如图示的装置进行实验,测定某电石试样中CaC2的质量分数,请回答下列问题:
(1)烧瓶中发生的反应的化学方程式
(2)为了得到比较平稳的乙炔气流,常可用
(3)装置B、C的作用是
(4)已知相同条件下,测得a g含CaC2 90%的样品与水完全反应产生的气体体积为b L.如果电石试样质量为c g,测得气体体积为d L,则电石试样中CaC2的质量分数计算式w(CaC2)=
考点:化学实验方案的评价,乙烯的实验室制法,乙炔炔烃,石油的分馏
专题:实验题,有机物的化学性质及推断
分析:I.(A)实验室制乙烯时,温度计测定反应液的温度,而石油分馏时测定馏分的温度;
(B)配制氢氧化铜悬浊液时,氢氧化钠溶液应过量;
(C)配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止,即为银氨溶液;
(D)发生强酸制取弱酸的反应比较苯酚、醋酸、碳酸的酸性强弱;
(E)Ag与稀硝酸反应,而浓硝酸易挥发;
(F)卤代烃与氢氧化钠溶液共热后,显碱性,应在酸性条件下再滴入硝酸银溶液,可检验卤原子的种类;
(G)苯酚溶于酒精;
II.(1)反应生成乙炔和氢氧化钙;
(2)水反应较快,而饱和食盐水可减缓反应速率;
(3)装置B、C为排水法测定乙炔的体积,注意在室温下测定气体体积,B中装满水等;
(4)a g含CaC2 90%的样品与水完全反应产生的气体体积为b L,则测得气体体积为d L,CaC2的质量为
g,以此计算.
(B)配制氢氧化铜悬浊液时,氢氧化钠溶液应过量;
(C)配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止,即为银氨溶液;
(D)发生强酸制取弱酸的反应比较苯酚、醋酸、碳酸的酸性强弱;
(E)Ag与稀硝酸反应,而浓硝酸易挥发;
(F)卤代烃与氢氧化钠溶液共热后,显碱性,应在酸性条件下再滴入硝酸银溶液,可检验卤原子的种类;
(G)苯酚溶于酒精;
II.(1)反应生成乙炔和氢氧化钙;
(2)水反应较快,而饱和食盐水可减缓反应速率;
(3)装置B、C为排水法测定乙炔的体积,注意在室温下测定气体体积,B中装满水等;
(4)a g含CaC2 90%的样品与水完全反应产生的气体体积为b L,则测得气体体积为d L,CaC2的质量为
| d×a×90% |
| b |
解答:
解:I.(A)实验室制乙烯时,温度计测定反应液的温度,而石油分馏时测定馏分的温度,则温度计水银球的位置不同,故正确;
(B)配制氢氧化铜悬浊液时,氢氧化钠溶液应过量,则应向NaOH溶液中滴加硫酸铜,故错误;
(C)配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止,即为银氨溶液,配制操作合理,故正确;
(D)醋酸与碳酸氢钠反应生成二氧化碳,二氧化碳与苯酚钠反应生成苯酚,排除醋酸的干扰,即可比较苯酚、醋酸、碳酸的酸性强弱,故正确;
(E)Ag与稀硝酸反应,而浓硝酸易挥发,则做过银镜反应的试管用稀硝酸清洗,故错误;
(F)卤代烃与氢氧化钠溶液共热后,显碱性,应在酸性条件下再滴入硝酸银溶液,可检验卤原子的种类,该选项没有在酸性条件下实验失败,故错误;
(G)苯酚溶于酒精,则若苯酚不慎沾到皮肤上,应立即用酒精洗涤,故正确;
故答案为:(B)(E)(F);
II.(1)反应生成乙炔和氢氧化钙,反应为CaC2+2H2O=C2H2↑+Ca(OH)2,故答案为:CaC2+2H2O=C2H2↑+Ca(OH)2;
(2)为了得到比较平稳的乙炔气流,常可用饱和食盐水代替水来减缓反应速率,故答案为:饱和食盐水;
(3)装置B、C的作用为排水法测定乙炔的体积,注意在反应后冷却室温下测定气体体积,B中装满水,且视线与凹液面最低点相平使测定体积准确,
故答案为:排水法测定乙炔的体积;反应后冷却室温下测定气体体积,B中装满水;
(4)a g含CaC2 90%的样品与水完全反应产生的气体体积为b L,则测得气体体积为d L,CaC2的质量为
g,则电石试样中CaC2的质量分数计算式w(CaC2)=
,故答案为:
.
(B)配制氢氧化铜悬浊液时,氢氧化钠溶液应过量,则应向NaOH溶液中滴加硫酸铜,故错误;
(C)配制银氨溶液时,向硝酸银溶液中逐滴滴加氨水,边滴边振荡,直到生成的沉淀溶解为止,即为银氨溶液,配制操作合理,故正确;
(D)醋酸与碳酸氢钠反应生成二氧化碳,二氧化碳与苯酚钠反应生成苯酚,排除醋酸的干扰,即可比较苯酚、醋酸、碳酸的酸性强弱,故正确;
(E)Ag与稀硝酸反应,而浓硝酸易挥发,则做过银镜反应的试管用稀硝酸清洗,故错误;
(F)卤代烃与氢氧化钠溶液共热后,显碱性,应在酸性条件下再滴入硝酸银溶液,可检验卤原子的种类,该选项没有在酸性条件下实验失败,故错误;
(G)苯酚溶于酒精,则若苯酚不慎沾到皮肤上,应立即用酒精洗涤,故正确;
故答案为:(B)(E)(F);
II.(1)反应生成乙炔和氢氧化钙,反应为CaC2+2H2O=C2H2↑+Ca(OH)2,故答案为:CaC2+2H2O=C2H2↑+Ca(OH)2;
(2)为了得到比较平稳的乙炔气流,常可用饱和食盐水代替水来减缓反应速率,故答案为:饱和食盐水;
(3)装置B、C的作用为排水法测定乙炔的体积,注意在反应后冷却室温下测定气体体积,B中装满水,且视线与凹液面最低点相平使测定体积准确,
故答案为:排水法测定乙炔的体积;反应后冷却室温下测定气体体积,B中装满水;
(4)a g含CaC2 90%的样品与水完全反应产生的气体体积为b L,则测得气体体积为d L,CaC2的质量为
| d×a×90% |
| b |
| da×90% |
| bc |
| da×90% |
| bc |
点评:本题考查化学实验方案的评价,为高频考点,涉及知识点较多,综合性较强,为拼凑型习题,综合考查学生分析能力、计算能力及知识综合应用能力等,把握物质性质及实验细节为解答的关键,注意实验操作的可行性、评价性分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将4.6g Cu和Mg完全溶于浓硝酸溶液中,反应中硝酸的还愿产物为4480ml NO2气和336ml N2O4气体(标准状况下),反应后的溶液中,加入过量NaOH溶液,生成沉淀的质量为( )
| A、9.02 g |
| B、8.51 g |
| C、8.26 g |
| D、7.04 g |
某原电池反应的离子方程式为:Fe+2H+=Fe2++H2↑.下列叙述正确的是( )
| A、电解质溶液可能为HNO3 |
| B、正极材料可能为Zn |
| C、正极材料可能为Cu |
| D、负极上:Fe失电子被还原 |
有9种物质:①甲烷 ②环己烷 ③环己烯 ④苯乙烯 ⑤聚乙烯 ⑥2-丁炔 ⑦苯 ⑧邻-二甲苯 ⑨Na2SO3溶液,其中既能使酸性KMnO4溶液褪色,又能因化学反应使溴水褪色的是( )
| A、③④⑥⑨ | B、③④⑥⑧ |
| C、③④⑤⑥⑨ | D、③④⑤⑥⑧ |
 鉴别失去标签的氯化钡、碳酸钠和稀盐酸三种无色溶液.
鉴别失去标签的氯化钡、碳酸钠和稀盐酸三种无色溶液.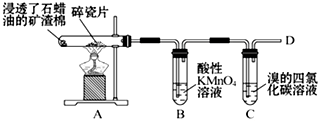 (1)如图是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,完成下列问题.
(1)如图是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,完成下列问题.