题目内容
将4.6g Cu和Mg完全溶于浓硝酸溶液中,反应中硝酸的还愿产物为4480ml NO2气和336ml N2O4气体(标准状况下),反应后的溶液中,加入过量NaOH溶液,生成沉淀的质量为( )
| A、9.02 g |
| B、8.51 g |
| C、8.26 g |
| D、7.04 g |
考点:氧化还原反应的计算,有关混合物反应的计算
专题:守恒法
分析:最终沉淀为氢氧化铜、氢氧化镁,铜和镁失去的电子的物质的量,等于硝酸被还原为二氧化氮、四氧化二氮获得的电子的物质的量,等于他们结合的氢氧根的物质的量,
根据氮的氧化物计算氢氧根的物质的量,沉淀的总质量=金属质量+氢氧根的质量.
根据氮的氧化物计算氢氧根的物质的量,沉淀的总质量=金属质量+氢氧根的质量.
解答:
解:本题涉及反应有:Cu
Cu2+
Cu(OH)2,Mg
Mg2+
Mg(OH)2,
反应后生成Cu(OH)2和Mg(OH)2,根据以上反应关系可知铜和镁失去的电子的物质的量等于结合的氢氧根的物质的量,
反应后沉淀的质量等于合金的质量加氢氧根离子的质量,
生成4480mL 的NO2气体和336mL的N2O4气体,反应中转移的电子的物质的量为
=0.23mol,
所以生成的沉淀的质量为4.6g+0.23mol×17g/mol=8.51g,
故选B.
| 失去2e- |
| 2OH- |
| 失去2e- |
| 2OH- |
反应后生成Cu(OH)2和Mg(OH)2,根据以上反应关系可知铜和镁失去的电子的物质的量等于结合的氢氧根的物质的量,
反应后沉淀的质量等于合金的质量加氢氧根离子的质量,
生成4480mL 的NO2气体和336mL的N2O4气体,反应中转移的电子的物质的量为
| 4.48L+0.336L×2 |
| 22.4L/mol |
所以生成的沉淀的质量为4.6g+0.23mol×17g/mol=8.51g,
故选B.
点评:本题考查氧化还原反应的计算,题目难度中等,本题解答的关键是铜和镁失去的电子的物质的量,等于他们结合的氢氧根的物质的量,而结合氢氧根的质量就正好是沉淀增加的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述正确的是( )
| A、锥形瓶可用作加热的反应器 |
| B、室温下,不能将浓硫酸盛放在铁桶中 |
| C、配制溶液定容时,俯视容量瓶刻度会使溶液的浓度偏高 |
| D、用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 |
下列操作中选择的仪器正确的是:( )
①分离汽油和氯化钠溶液 ②从含Fe3+的自来水中得到蒸馏水 ③分离氯化钾和二氧化锰混合物 ④从氯化钠溶液中得到氯化钠晶体
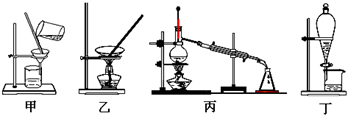
①分离汽油和氯化钠溶液 ②从含Fe3+的自来水中得到蒸馏水 ③分离氯化钾和二氧化锰混合物 ④从氯化钠溶液中得到氯化钠晶体

| A、①-丁 ②-丙 ③-甲 ④-乙 |
| B、①-乙 ②-丙 ③-甲 ④-丁 |
| C、①-丁 ②-丙 ③-乙 ④-甲 |
| D、①-丙 ②-乙 ③-丁 ④-甲 |
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A、pH=1的溶液中:Na+、K+、MnO4-、CO32- |
| B、c(H+)=1×10-13mol?L-1的溶液中:Mg2+、Cu2+、SO42-、NO3- |
| C、0.1mol?L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl- |
| D、0.1mol?L-1FeCl3溶液中:Fe2+、NH4+、SCN-、SO42- |
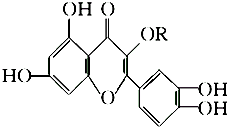 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )| A、最多可以和含6 molBr2的溴水反应 |
| B、可用有机溶剂萃取 |
| C、分子中有三个苯环 |
| D、1 mol 维生素P可以和4 mol NaOH反应 |
某有机物的结构如图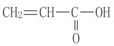 ,它不具有的官能团是( )
,它不具有的官能团是( )
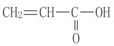 ,它不具有的官能团是( )
,它不具有的官能团是( )A、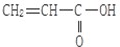 |
| B、-OH |
| C、 |
| D、-Cl |
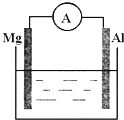 (1)如图所示,烧杯中的溶液为稀硫酸,则观察到的现象为
(1)如图所示,烧杯中的溶液为稀硫酸,则观察到的现象为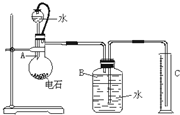 I.下列有关实验的说法不正确的是
I.下列有关实验的说法不正确的是