题目内容
7.下列说法正确的是( )| A. | 物质的摩尔质量等于其相对原子质量或相对分子质量 | |
| B. | 摩尔是7个基本物理量之一 | |
| C. | 46 g NO2和N2O4的混合物中含有的氮原子数为NA | |
| D. | 1molCO2所占的体积约为22.4L |
分析 A.摩尔质量与相对分子质量、相对原子量的单位不同;
B.摩尔为物质的量单位,不是物理量;
C.根据最简式NO2计算混合气体中含有氮原子数目;
D.没有告诉在标况下,不能使用标况下的气体摩尔体积计算.
解答 解:A.摩尔质量的单位为g/mol,相对原子质量和相对分子质量没有单位,而不相等,故A错误;
B.物质的量是7个基本物理量之一,摩尔是物质的量单位,故B错误;
C.46 gNO2和N2O4的混合物中含有46g最简式NO2,含有最简式NO2的物质的量为:$\frac{46g}{46g/mol}$=1mol,则混合物中含有1molN原子,含有的氮原子数为NA,故C正确;
D.不是标况下,不能使用标况下的气体摩尔体积计算二氧化碳的体积,故D错误;
故选C.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔、摩尔质量与相对分子质量之间的关系为解答关键,试题培养了学生的灵活应用基础知识的能力.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
2.将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述不正确的是( )
| A. | 反应速率:前者快,后者慢 | |
| B. | 消耗硝酸的物质的量:前者多,后者少 | |
| C. | 反应生成相同条件下气体的体积:前者多,后者少 | |
| D. | 反应中转移的电子总数:前者多,后者少 |
12.炼金废水中所含CN-有剧毒,其性质与卤素离子相似,还原性介于I-与Br-之间,HCN为弱酸.下列说法不正确的是( )
| A. | CN-可以和稀硫酸反应生成HCN | B. | CN-可被Cl2氧化成(CN)28 | ||
| C. | 在水溶液中(CN)2可被F-还原 | D. | HCN的电子式为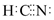 |
19.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向Al2(SO4)3溶液中加入过量NH3•H2O:Al3++4NH3•H2O═-+4NH4+ | |
| B. | 铅酸蓄电池充电时的正极反应:PbO2+4H++SO42-+2e-═PbSO4+2H2O | |
| C. | Fe2(SO4)3溶液与Ba(OH)2溶液反应:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ | |
| D. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:2NH4++Fe2++4OH-═Fe(OH)2↓+2NH3•H2O |
14.在2L的密闭容器中进行下列反应:A(g)+2B(g)?2C(g)+D(g)起始投入1mol A和2mol B,在一定条件下反应建立平衡,若条件不变,按下列各组物质加入起始物质,再次达到平衡后可能维持c(A)=c(B)=c(C)=0.2mol/L的一组是( )
| A. | 1mol A+2mol B+1mol C | |
| B. | 0.6mol C+0.6mol D+0.2mol B+0.3mol A | |
| C. | 0.6mol A+0.2mol D+0.1mol C | |
| D. | 0.25mol A+0.5mol B+0.1mol C |