��Ŀ����
15���Լ���Ϊ��ʼԭ����ȡ��������һ��Ƚϳ���ļ�������������ȡ����������ͼ��ͼ1��������Ϣ�ش��������⣺
��1����I�����ķ�ӦΪCH4��g��+H2O��g��?CO��g��+3H2��g����
��д���÷�Ӧ��ƽ�ⳣ������ʽ$\frac{c��CO����{c}^{3}��{H}_{2}��}{c��C{H}_{4}����c��{H}_{2}O��}$��
����֪�ڡ�ˮ̼�ȡ�$\frac{c��{H}_{2}O��}{c��C{H}_{4}��}$=3ʱ������¶ȣ�T ����ѹǿ��p����������Ӧ��Ӱ����ͼ2��ʾ���������¶ȣ��÷�Ӧ��ƽ�ⳣ��K�������������С�����䡱������ͼ��֪P1��P2�������������������=����
��2�������ķ�ӦΪCO��g��+H2O��g��?CO2��g��+H2 ��g����T1�¶�ʱ����2L�ĺ����ܱ�������ͨ��һ������CO��H2O��g������Ӧ�����в�ò������������ʾ������t1��t2����
| ��Ӧʱ�䣨min�� | n��CO����mol�� | N��H2O����mol�� |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
�����ﵽƽ����������������䣬ֻ����ԭƽ����ϵ����ͨ��0.20mol H2O��g����������˵����ȷ����ab��
a��CO��ת���ʽ����� b��H2O��g�����������������
c��������ܶȽ����� d����ѧƽ�ⳣ��������
���� ��1����ƽ�ⳣ��Ϊ������ƽ��Ũ�Ȼ�ѧ�������ݳ˻��뷴Ӧ��ƽ��Ũ�Ȼ�ѧ�������ݳ˻�֮�ȣ�
����ͼ��ʼ�������¶ȼ�������������С��˵�������¶�ƽ�������ƶ���ƽ�ⳣ������
����ӦΪ�������ʵ�������ķ�Ӧ������ѹǿƽ�������ƶ�������������������
��2����t1minʱ����Ӧ��COΪ1.2mol-0.8mol=0.4mol���ɷ���ʽ��֪��Ӧ��ˮΪ0.4mol�����ʱˮ�����ʵ���Ϊ0.6mol-0.4mol=0.2mol����t2minʱˮΪ0.2mol����t1min��t2min������ƽ��״̬��ƽ��ʱ������̼Ϊ0.4mol��
����T1�¶Ȳ��䣬����ԭ������ͨ�� 0.60mol CO��1.20mol H2O��g������ԭƽ����ȷ�Ӧ���������������߰�1��1��Ӧ��ƽ�ⳣ��K=$\frac{c��C{O}_{2}����c��{H}_{2}��}{c��CO����c��{H}_{2}O��}$���䣬��ƽ��ʱ��Ӧ�����������ԭƽ����ͬ��
�����ﵽƽ����������������䣬ֻ����ԭƽ����ϵ����ͨ��0.20mol H2O��g����
a��ƽ�������ƶ���CO��ת���ʽ�����
b����ЧΪ��ʼͨ��1.6molCO��0.8molˮ����ƽ���������0.4molCO������ʼͨ��1.6molCO��0.8molˮ��ԭƽ��Ϊ��Чƽ�⣬ƽ��ʱˮ�����������ͬ��
c��������������������������ݻ����䣻
d����ѧƽ�ⳣ��ֻ���¶�Ӱ�죮
��� �⣺��1����CH4��g��+H2O��g��?CO��g��+3H2��g����ƽ�ⳣ������ʽK=$\frac{c��CO����{c}^{3}��{H}_{2}��}{c��C{H}_{4}����c��{H}_{2}O��}$��
�ʴ�Ϊ��$\frac{c��CO����{c}^{3}��{H}_{2}��}{c��C{H}_{4}����c��{H}_{2}O��}$��
����ͼ��ʼ�������¶ȼ�������������С��˵�������¶�ƽ�������ƶ���ƽ�ⳣ������
����ӦΪ�������ʵ�������ķ�Ӧ������ѹǿƽ�������ƶ���������������������P1��P2��
�ʴ�Ϊ��������
��2����t1minʱ����Ӧ��COΪ1.2mol-0.8mol=0.4mol���ɷ���ʽ��֪��Ӧ��ˮΪ0.4mol�����ʱˮ�����ʵ���Ϊ0.6mol-0.4mol=0.2mol����t2minʱˮΪ0.2mol����t1min��t2min������ƽ��״̬��ƽ��ʱ������̼Ϊ0.4mol��
����T1�¶Ȳ��䣬����ԭ������ͨ�� 0.60mol CO��1.20mol H2O��g������ԭƽ����ȷ�Ӧ���������������߰�1��1��Ӧ��ƽ�ⳣ��K=$\frac{c��C{O}_{2}����c��{H}_{2}��}{c��CO����c��{H}_{2}O��}$���䣬��ƽ��ʱ��Ӧ�����������ԭƽ����ͬ�������ɶ�����̼Ϊ0.4mol��
�ʴ�Ϊ��0.4mol��
�����ﵽƽ����������������䣬ֻ����ԭƽ����ϵ����ͨ��0.20mol H2O��g����
a��ƽ�������ƶ���CO��ת���ʽ�����a��ȷ��
b����ͨ��0.20mol H2O��g����ЧΪ��ʼͨ��1.6molCO��0.8molˮ����ƽ���������0.4molCO������0.4molCO���ƽ���뿪ʼͨ��1.6molCO��0.8molˮ����ƽ����ȣ�ƽ�������ƶ���ˮ���������������ʼͨ��1.6molCO��0.8molˮ��ԭƽ��Ϊ��Чƽ�⣬ƽ��ʱˮ�����������ͬ������ԭƽ����ϵ����ͨ��0.20mol H2O��g��ʱ��H2O��g�����������������b��ȷ��
c��������������������������ݻ����䣬�ܶ�����c����
d���¶Ȳ��䣬ƽ�ⳣ�����䣬��d����
��ѡ��ab��
���� ���⿼�黯ѧƽ����㡢��ѧƽ��Ӱ�����صȣ���2���Т�ע��Թ��ɹ����ܽᣬ��2���Т�bѡ��ע�����õ�Ч˼�빹��ƽ�⽨����;�����Ѷ��еȣ�

| A�� | ����ƿ����ˮ��δ�������ﴦ�� | |
| B�� | ����ʱ�����ӿ̶��� | |
| C�� | ����Ͳ��ȡŨ����ʱ����ˮϴ����Ͳ2��3�Σ�ϴҺ�����ձ��� | |
| D�� | ���ݺ�ת����ƿ���Σ�����Һ����͵���ڿ̶��ߣ��ٲ��Ӽ���ˮ���̶��� |
��1���û���̿��ԭ��������������йط�ӦΪ��C��s��+2NO��g��?N2��g��+CO2��g����
ij�о�С����һ�������ݻ�Ϊ3L���ݻ�������ܱ������������������������Բ��ƣ��м���NO�������Ļ���̿���ں��£�T1�棩�����·�Ӧ����ò�ͬʱ�䣨t��ʱ�����ʵ����ʵ�����n�������
| n/mol t/min | NO | N2 | CO2 |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | 0.42 | 0.42 |
| 20 | 0.80 | 0.60 | 0.60 |
| 30 | 0.80 | 0.60 | 0.60 |
�ڸ��ݱ������ݣ�����T1��ʱ�÷�Ӧ��ƽ�ⳣ��Ϊ0.56��������λС��������ijһʱ�̣���������1.2molC��1.2molNO��0.75molN2��1.08molCO2����ʱv������=v���棩�����������=����
�����и������жϸ÷�Ӧ�ﵽƽ��״̬����AC���������ĸ����
A��v��NO��������=2v��N2�����棩 B��������CO2��N2�������Ϊ1��1
C����������ƽ����Է����������ֲ��� D��������ѹǿ���ֲ���
��һ���¶��£�����NO����ʼŨ��������NO��ƽ��ת���ʲ��䣨����������䡱��С������
��2����ˮ����ͨ�����ȵ�̼���ɲ���ˮú������֪��C��s��+H2O��g��?CO��g��+H2��g����H=+131.3kJ•mol-1��C��s��+CO2��g��?2CO��g����H=+172.5kJ•mol-1����CO��g��+H2O��g��?CO2��g��+H2��g�����ʱ��H=-41.2kJ•mol-1��
��3����3L�ݻ��ɱ���ܱ������з���������Ӧ��H2��g��+CO2��g��?H2O��g��+CO��g����������c��CO���淴Ӧʱ��t�仯�����ߢ���ͼ��ʾ��
������t0ʱ�ı�һ��������ʹ���ߢ������ߢ���ı�������Ǽ��������
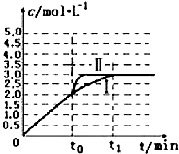
������t0ʱ�̽������������ѹ����2L�������������䣩������ͼ�л���c��CO���淴Ӧʱ��t�仯�����ߣ�
| A�� | �ӳɷ�Ӧ | B�� | ������Ӧ | C�� | ˮ�ⷴӦ | D�� | ���۷�Ӧ |

 ���ϳɡ�ˮ�ȴ��������ˡ�ˮϴ�����洦��������ˮϴ������
���ϳɡ�ˮ�ȴ��������ˡ�ˮϴ�����洦��������ˮϴ������
 �״���ˮ�ʻ����һ������Ⱦ����һ�ֵ绯ѧ��������������Ⱦ����ԭ����ͨ���Co2+������Co3+��Ȼ����Co3+����������ˮ�еļ״�������CO2��������ʵ��������ͼװ��ģ���������̣�
�״���ˮ�ʻ����һ������Ⱦ����һ�ֵ绯ѧ��������������Ⱦ����ԭ����ͨ���Co2+������Co3+��Ȼ����Co3+����������ˮ�еļ״�������CO2��������ʵ��������ͼװ��ģ���������̣�