题目内容
7.配制250mL 0.1mol•L-1盐酸溶液时,下列实验操作会使配制溶液浓度偏低的是( )| A. | 容量瓶内有水,未经过干燥处理 | |
| B. | 定容时,仰视刻度线 | |
| C. | 用量筒量取浓盐酸时,用水洗涤量筒2~3次,洗液倒入烧杯中 | |
| D. | 定容后倒转容量瓶几次,发现液体最低点低于刻度线,再补加几滴水到刻度线 |
分析 根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析.
解答 解:A、只要定容时正确,至于水是原来就有的还是后来加入的,对浓度无影响,即容量瓶未干燥即用来配制溶液,对溶液浓度无影响,故A错误;
B、定容时,仰视刻度线,则溶液体积偏大,浓度偏高,故B错误;
C、量筒的洗涤液应注入废液缸中,若注入容量瓶中,则溶质的物质的量偏多,则浓度偏高,故C错误;
D、定容后液面低于刻度线是正常的,若再加水至刻度线,则溶液浓度偏低,故D正确.
故选D.
点评 本题考查了一定物质的量浓度溶液的配制过程中的误差分析,属于基础型题目,难度不大.

练习册系列答案
 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案
相关题目
17.下列实验方案能达到实验目的是( )
| A. |  用图所示装置,蒸干AlCl3饱和溶液制备AlCl3晶体 | |
| B. |  用图所示装置,制备并收集少量NO2气体 | |
| C. |  用图所示装置,可用于制备和收集乙酸乙酯 | |
| D. | 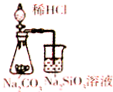 用图所示装置,证明非金属性强弱:Cl>C>Si |
18.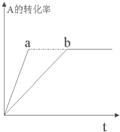 已知某可逆反应在密闭容器中进行:A(g)+2B(g)?3C(g)+D(s)(放热反应),图中曲线b代表一定条件下该反应的过程,若使曲线b变为曲线a,可采取的措施是( )
已知某可逆反应在密闭容器中进行:A(g)+2B(g)?3C(g)+D(s)(放热反应),图中曲线b代表一定条件下该反应的过程,若使曲线b变为曲线a,可采取的措施是( )
 已知某可逆反应在密闭容器中进行:A(g)+2B(g)?3C(g)+D(s)(放热反应),图中曲线b代表一定条件下该反应的过程,若使曲线b变为曲线a,可采取的措施是( )
已知某可逆反应在密闭容器中进行:A(g)+2B(g)?3C(g)+D(s)(放热反应),图中曲线b代表一定条件下该反应的过程,若使曲线b变为曲线a,可采取的措施是( )| A. | 增大A的浓度 | B. | 扩大容器的容积 | C. | 加入催化剂 | D. | 升高温度 |
15.分液漏斗在使用前,必须进行的操作是( )
| A. | 打开活塞 | B. | 拔下玻璃塞 | C. | 检查是否漏水 | D. | 检查是否干燥 |
2.下列说法中正确的是( )
| A. | CCl4的比例模型示意图为 | B. |  的名称为2,6-二甲基3乙基庚烷 的名称为2,6-二甲基3乙基庚烷 | ||
| C. | 化合物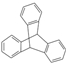 有4种一氯代物 有4种一氯代物 | D. | 1mol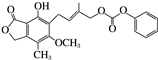 最多能与4molNaOH完全反应 最多能与4molNaOH完全反应 |
12.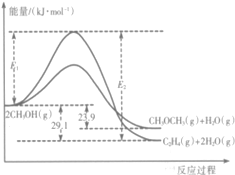 醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:
醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:
i.2CH3OH(g)?CH3OCH3(g)+H2O(g)
ii.2CH3OH(g)?C2H4(g)+2H2O(g)
I.上述反应过程中能量变化如图所示:
(1)在某密闭容器中,充人一定量CH3OH(g)发生上述两个反应,反应i(填“i”或“ii”)的速率较大,其原因为该反应的活化能较小.若在容器中加入催化剂,使ii的反应速率增大,则E1和E2-E1的变化是:E1减小;E2-E1不变(填“增大”、“减小”或“不变”).
(2)已知:CH3CH2OH(g)=CH3OCH3(g)△H=+50.7kJ/mol.则乙烯气相直接水合反应C2H4(g)+H2O(g)═C2H5OH(g)的△H=-45.5kJ•mol-1.
Ⅱ,某研究小组通过控制反应条件,在三个容积均为2L的密闭容器中只发生反应i,起始反应温度均为T℃,起始投料如下表所示:
(3)比较平衡时容器1中c1(H2O)和容器2中c2(H2O)的大小:c1(H2O)<c2(H2O)(填“>”、“<”或“=”);三个容器中反应的化学平衡常数分别记为K1、K2和K3,三者的大小关系为K1=K2>K3.
(4)若容器l中平衡时CH3OH(g) 的转化率为80%,则该温度下反应i的平衡常数K=4.
 醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:
醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:i.2CH3OH(g)?CH3OCH3(g)+H2O(g)
ii.2CH3OH(g)?C2H4(g)+2H2O(g)
I.上述反应过程中能量变化如图所示:
(1)在某密闭容器中,充人一定量CH3OH(g)发生上述两个反应,反应i(填“i”或“ii”)的速率较大,其原因为该反应的活化能较小.若在容器中加入催化剂,使ii的反应速率增大,则E1和E2-E1的变化是:E1减小;E2-E1不变(填“增大”、“减小”或“不变”).
(2)已知:CH3CH2OH(g)=CH3OCH3(g)△H=+50.7kJ/mol.则乙烯气相直接水合反应C2H4(g)+H2O(g)═C2H5OH(g)的△H=-45.5kJ•mol-1.
Ⅱ,某研究小组通过控制反应条件,在三个容积均为2L的密闭容器中只发生反应i,起始反应温度均为T℃,起始投料如下表所示:
| 编号 起始投料/mol | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| 恒温容器1 | 2 | 0 | 0 |
| 恒温容器2 | 0 | 2 | 2 |
| 绝热容器3 | 2 | 0 | 0 |
(4)若容器l中平衡时CH3OH(g) 的转化率为80%,则该温度下反应i的平衡常数K=4.
16.下列反应的离子方程式中正确的是( )
| A. | 将Al条投入NaOH溶液中:Al+OH-+H2O═AlO${\;}_{2}^{-}$+H2↑ | |
| B. | 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | |
| C. | 向CuSO4溶液中加入Na2O2:Na2O2+2Cu2++2H2O═2Na++2Cu(OH)2↓+O2↑ | |
| D. | 将0.2 mol/L的NH4Al(SO4)2溶液与0.3 mol/L的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
15.以甲烷为初始原料制取氢气,是一项比较成熟的技术,下面是制取氢气的流程图如图1,根据信息回答下列问题:
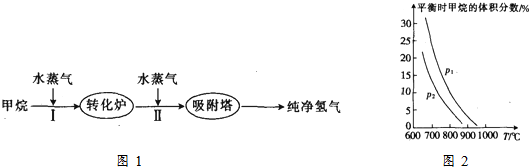
(1)阶段I发生的反应为CH4(g)+H2O(g)?CO(g)+3H2(g).
①写出该反应的平衡常数表达式$\frac{c(CO)×{c}^{3}({H}_{2})}{c(C{H}_{4})×c({H}_{2}O)}$;
②已知在“水碳比”$\frac{c({H}_{2}O)}{c(C{H}_{4})}$=3时,测得温度(T )和压强(p)对上述反应的影响如图2所示.则升高温度,该反应的平衡常数K增大(填“增大”、“减小”或“不变”),据图可知P1>P2.(填“>”、“<”或“=”)
(2)阶段Ⅱ发生的反应为CO(g)+H2O(g)?CO2(g)+H2 (g),T1温度时,向2L的恒容密闭容器中通入一定量的CO和H2O(g),反应过程中测得部分数据如表所示(表中t1<t2):
①保持T1温度不变,若向原容器中通入 0.60mol CO和1.20mol H2O(g),则达到平衡后n(CO2)=0.4mol.
②若达到平衡后,保持其他条件不变,只是向原平衡体系中再通入0.20mol H2O(g),则下列说法正确的是ab.
a、CO的转化率将增大 b、H2O(g)的体积分数将增大
c、气体的密度将不变 d、化学平衡常数将增大.

(1)阶段I发生的反应为CH4(g)+H2O(g)?CO(g)+3H2(g).
①写出该反应的平衡常数表达式$\frac{c(CO)×{c}^{3}({H}_{2})}{c(C{H}_{4})×c({H}_{2}O)}$;
②已知在“水碳比”$\frac{c({H}_{2}O)}{c(C{H}_{4})}$=3时,测得温度(T )和压强(p)对上述反应的影响如图2所示.则升高温度,该反应的平衡常数K增大(填“增大”、“减小”或“不变”),据图可知P1>P2.(填“>”、“<”或“=”)
(2)阶段Ⅱ发生的反应为CO(g)+H2O(g)?CO2(g)+H2 (g),T1温度时,向2L的恒容密闭容器中通入一定量的CO和H2O(g),反应过程中测得部分数据如表所示(表中t1<t2):
| 反应时间(min) | n(CO)(mol) | N(H2O)(mol) |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
②若达到平衡后,保持其他条件不变,只是向原平衡体系中再通入0.20mol H2O(g),则下列说法正确的是ab.
a、CO的转化率将增大 b、H2O(g)的体积分数将增大
c、气体的密度将不变 d、化学平衡常数将增大.