题目内容
12.某直链一元醇14g能与金属钠完全反应,生成0.2克H2,则此醇的同分异构体数目为( )| A. | 6个 | B. | 7个 | C. | 8个 | D. | 9个 |
分析 醇和钠反应,生成氢气,实际反应的方程式是2ROH+2Na=2RONa+H2,0.2g氢气是0.1mol,根据方程式可求出醇的物质的量,再求出醇的分子量,根据相对分子质量确定分子式,然后确定醇的分子式书写可能的同分异构体.
解答 解:(1)醇和钠反应,生成氢气,实际反应的方程式是2ROH+2Na=2RONa+H2,0.2g氢气是0.1mol,醇的物质的量为0.1×2=0.2mol,醇的摩尔质量M=$\frac{m}{n}$=$\frac{14g}{0.2mol}$=70g/mol,相对分子质量为70,烃基R的相对分子质量为:70-17=53,$\frac{53}{14}$=4余-3,所以该醇的分子式为 C4H6O,为炔醇或二烯醇,可能结构简式为:
CH≡C-CH2-CH2OH、CH≡C-CHOH-CH3、HO-C≡C-CH2-CH3、CH3-C≡C-CH2OH、CH2=CH-CH=CHOH、CH2=C(OH)-CH=CH2;CH2=C=CH-CH2OH、CH2=C=C(OH)-CH3、
CH(OH)=C=CH-CH3;
故选D.
点评 本题考查化学方程式的有关计算及同分异构体的书写,中等难度,计算出分子式是解题关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH同时得到某种副产物,其原理如图所示(电极材料为石墨).下列说法不正确的是( )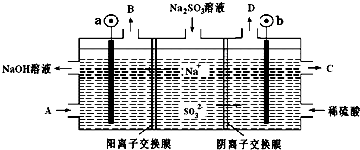

| A. | b电极上的主反应是 SO32--2e-+H2O═SO42-+2H+ | |
| B. | 若D是混合气体,则可能含有SO2、O2等成分 | |
| C. | a 电极发生还原反应,当有1mol Na+通过阳离子交换膜时,a极生成11.2L气体 | |
| D. | A溶液是稀NaOH溶液,作用是增强溶液的导电性;C是较浓的硫酸溶液 |
3.NA表示阿伙加德罗常数的值.下列判断正确的是( )
| A. | 常温常压下,17g氨气分子所含质子数为10NA | |
| B. | 1mol CL2参加反应,转移电子数一定为2N | |
| C. | 常温常压下,22.4 L C02分子中含有2NA个σ键和2NA个1π键 | |
| D. | 1 L 0.01 mol.L-1的Na2CO3溶液中含有0.01NA个CO2- |
20.下列气态氢化物中最稳定的是( )
| A. | PH3 | B. | NH3 | C. | H2O | D. | CH4 |
5.在一定温度下,将气体X和气体Y各0.16mol充入10L 恒容密闭容器中,发生反应:X(g)+Y(g)═2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2min的平均速率ν(Z)=2.0×10-5 mol/(L•min) | |
| B. | 4min时,ν(逆)>ν(正) | |
| C. | 该温度下,此反应的平衡常数K=1.44 | |
| D. | 7min时,反应还未达到平衡状态 |
2.化学与人类生产、生活、社会可持续发展密切相关,下列说法不正确的是( )
| A. | 光化学烟雾是氮氧化物受紫外线照射后与空气中的一些碳氢化合物作用后生成的一种有毒烟雾 | |
| B. | 以粮食为原料酿酒过程的变化包括粮食→淀粉→葡萄糖→乙醇 | |
| C. | 航天飞机上使用的隔热陶瓷瓦,大多是以碳纤维做增强体的新型复合材料 | |
| D. | 绿色化学的核心是应用化学原理对环境污染进行治理 |
3.下列各组粒子,核外电子总数和质子总数均相同的是( )
| A. | S2-和HS- | B. | H3O+和OH- | C. | Na+和NH${\;}_{4}^{+}$ | D. | K+和Ne |