题目内容
3.下列各组粒子,核外电子总数和质子总数均相同的是( )| A. | S2-和HS- | B. | H3O+和OH- | C. | Na+和NH${\;}_{4}^{+}$ | D. | K+和Ne |
分析 利用阳离子中的核外电子数为质子数之和减去电荷数,阴离子中的核外电子数为质子数之和加上微粒的电荷数,分子中的核外电子数之和=质子数之和来解答.
解答 解:A、S2-的质子数为16,核外电子总数为18,HS-的质子数为17,核外电子总数为18,故A错误;
B、H3O+的质子数为19,核外电子总数为18,OH-的质子数为17,核外电子总数为18,故B错误;
C、Na+的质子数为11,核外电子总数为10,NH4+的质子数为11,核外电子总数为10,故C正确;
D、K+的质子数为19,核外电子总数为18,Ne的质子数为10,核外电子总数为10,故D错误;
故选:C.
点评 本题主要考查了微粒中质子数和电子数的计算,根据微粒的构成情况确定质子数和电子数,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.某直链一元醇14g能与金属钠完全反应,生成0.2克H2,则此醇的同分异构体数目为( )
| A. | 6个 | B. | 7个 | C. | 8个 | D. | 9个 |
14.LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车.电池反为:FePO4+Li═LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质.下列有关LiFePO4电池说法正确的是( )
| A. | 可加入硫酸以提高电解质的导电性 | |
| B. | 放电时电池内部Li+向负极移动 | |
| C. | 充电过程中,电池正极材料的质量增加 | |
| D. | 放电时电池正极反应为:FePO4+Li++e-═LiFePO4 |
11.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,40 g SO3所含的氧原子的数目为1.5 NA | |
| B. | 5.6 g铁与足量氯气或硫蒸气反应转移的电子数均为0.3 NA | |
| C. | 12.5 mL 16 mol•L-1浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA | |
| D. | 常温下5.6 g铁投入到足量浓硝酸中反应,转移电子数为0.3 NA |
18.甲酸的下列性质中,可以证明它是弱电解质的是( )
| A. | 1 mol•L-1甲酸溶液的pH约为2 | |
| B. | 甲酸能与水以任意比例互溶 | |
| C. | 10 mL 1 mol•L-1甲酸恰好与10 mL 1 mol•L-1 NaOH溶液完全反应 | |
| D. | 甲酸溶液的导电性比强酸溶液弱 |
12.四种常见元素的相关信息如下表所示,请回答下列问题:
(1)W的基态原子的价电子排布式为4s24p3,Z、W两种元素的第一电离能的大小关系为Cl>As(用元素符号表示).
(2)Z能与X、Y、W形成XZ4、YZ3、WZ3、WZ5等化合物,其中中心原子杂化方式为sp3的分子是CCl4、NCl3、AsCl3(填化学式,下同),分子构型为正四面体的是CCl4.
(3)Y、Z及氢、铂元素可组成为Pt(YH3)2Z2的配合物,该配合物存在两种不同的结构:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大.
①Q是非极性分子(填“极性”或“非极性”).
②P分子的结构简式为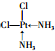 (YH3作为一个整体写)
(YH3作为一个整体写)
(4)X的一种单质分子(N)的球棍模型如图1所示,该分子中每个X原子均形成了稳定的8电子结构,则分子中σ键与π键数目之比为3:1.一定条件下含NA个X原子的N与足量氢气发生加成反应时,消耗1gH2
(5)W与镓的化合物(GaW)是一种半导体材料,其晶胞结构如图2所示,镓原子的配位数是4,该晶胞的密度为ρg•cm-3,则该晶胞的边长为$\root{3}{\frac{580}{ρ•{N}_{A}}}$cm(用含NA、ρ的代数式表示).

图1 图2.
| 元素 | X | Y | Z | W |
| 相关信息 | 短周期p区元素,有种单质常作电极材料 | 基态原子2p能级上各轨道中均有电子且电子的自旋方向相同 | 基态原子的核外电子共有17种运动状态 | 位于第四周期第VA族 |
(2)Z能与X、Y、W形成XZ4、YZ3、WZ3、WZ5等化合物,其中中心原子杂化方式为sp3的分子是CCl4、NCl3、AsCl3(填化学式,下同),分子构型为正四面体的是CCl4.
(3)Y、Z及氢、铂元素可组成为Pt(YH3)2Z2的配合物,该配合物存在两种不同的结构:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大.
①Q是非极性分子(填“极性”或“非极性”).
②P分子的结构简式为
 (YH3作为一个整体写)
(YH3作为一个整体写)(4)X的一种单质分子(N)的球棍模型如图1所示,该分子中每个X原子均形成了稳定的8电子结构,则分子中σ键与π键数目之比为3:1.一定条件下含NA个X原子的N与足量氢气发生加成反应时,消耗1gH2
(5)W与镓的化合物(GaW)是一种半导体材料,其晶胞结构如图2所示,镓原子的配位数是4,该晶胞的密度为ρg•cm-3,则该晶胞的边长为$\root{3}{\frac{580}{ρ•{N}_{A}}}$cm(用含NA、ρ的代数式表示).

图1 图2.
 ;DB2有多种重要的用途,请你写出其中的一种:制玻璃、制光导纤维、制粗硅(其中一种).
;DB2有多种重要的用途,请你写出其中的一种:制玻璃、制光导纤维、制粗硅(其中一种).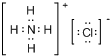 .
.