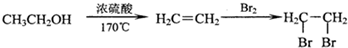题目内容
13.某含Na+的溶液中还可能含有NH4+、Fe3+、Mg2+、Br-、CO32-、SO32-.取样,滴加足量氯水有气泡产生,溶液呈橙色;向橙色溶液中加BaCl2溶液无现象.为确定该溶液的组成,还需进行的实验有( )| A. | 取样,加氯水和CCl4,振荡、静置 | |
| B. | 取样,加足量的NaOH浓溶液,加热,用湿润的红色石蕊试纸检验气体 | |
| C. | 取样,加足量盐酸加热,用湿润的品红试纸检验气体 | |
| D. | 取样,滴加硫氰化钾溶液 |
分析 ①向溶液中滴加足量氯水后,溶液变橙色,说明溶液中含有Br-,且有无色气泡冒出,说明溶液中含离子CO32-或SO32-离子,那么与其混合生成沉淀的不能存在;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成,说明不含SO32-,据此进行解答.
解答 解:①向溶液中滴加足量氯水后,溶液变橙色,说明溶液中含有Br-,且有气泡冒出,说明溶液中含离子CO32-或SO32-;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成,说明不含SO32-,那么一定含有:CO32-,一定不能含有与碳酸根生成沉淀的离子:Fe3+、Mg2+,通过以上分析,还不能证明NH4+是否存在,铵根离子的检验可以采用加入强碱加热的方法,取样,加足量的NaOH浓溶液,加热,用湿润的红色石蕊试纸检验气体,若试纸变蓝,证明含有铵根离子,
故选B.
点评 本题考查离子的检验及离子共存问题,题目难度中等,注意掌握常见离子的性质及检验方法,明确常见离子的反应的现象,然后结合离子的性质进行判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.当光束通过下列分散系时,可观察到丁达尔效应的是( )
| A. | 乙醇溶液 | B. | 氨化钠溶液 | C. | 盐酸 | D. | 氢氧化铁胶体 |
1.将ag乙醇(分子式为C2H6O)充分燃烧,将燃烧生成的气体(150℃)通过盛有过量Na2O2的干燥管(反应气体无损失),充分反应后干燥管增重bg,则a和b的关系为( )
| A. | a>b | B. | a=b | C. | a<b | D. | 无法比较 |
8.将Cu片放入0.1mol•L-1FeCl3溶液中,反应一定时间后取出Cu片,溶液中c(Fe3+):c(Fe2+)=2:1,则Cu2+与原溶液中的Fe3+的物质的量之比为( )
| A. | 4:1 | B. | 1:4 | C. | 1:6 | D. | 6:1 |
5.光纤通讯的光导纤维是由下列哪种物质经特殊工艺制成( )
| A. | 石墨 | B. | 二氧化硅 | C. | 氧化镁 | D. | 硅 |
2.工业上以氯气和石灰乳为原料制造漂白粉.漂白粉的有效成分是( )
| A. | Cl2 | B. | CaCl2 | C. | Ca(OH)2 | D. | Ca(ClO)2 |
3.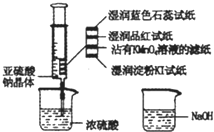 如图,在注射器中加人少量Na2SO3晶体,并吸人少f浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
如图,在注射器中加人少量Na2SO3晶体,并吸人少f浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
 如图,在注射器中加人少量Na2SO3晶体,并吸人少f浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
如图,在注射器中加人少量Na2SO3晶体,并吸人少f浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )| A. | 湿润淀粉碘化钾试纸未变蓝说明SO2不能将I-还 原为I2 | |
| B. | 品红试纸、沾有KMnO4溶液的滤纸均褪色证明了SO2具有漂白性 | |
| C. | 实验后,可把注射器中的物质推人NaOH溶液,以减少环境污染 | |
| D. | 蓝色石蕊试纸先变红后褪色 |
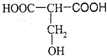 .
. +2H2O;
+2H2O;