题目内容
2.用经疏酸酸化处理的三氧化铬(Cr03)硅胶测试司机呼出的气体,根据桂胶颜色的变化可以判断司机是否酒驾.测试过程中乙醉被氧化为乙醛,乙醛还可被氧化为乙酸.(1)铬原子基态核外电子排布式为[Ar]3d54s1或1s22s22p63s23p63d54s1.
(2)lmol乙酸分子中含有<r键的数目为 mol.
(3)乙醛中碳原子轨道的杂化类型是sp2,sp3.
(4)乙醉与乙醛的相对分子质量相差不大,但乙醇的沸点(78.5℃)却比乙醛的沸点(20.8℃)高出许多,是因为乙醇分子间存在氢键,而乙醛分子间不存在氢键.
(5)与SO42-互为等电子体的阴离子为PO43-或SiO44-(任写一种).
(6)已知Cr(0H)3在碱性较强的溶液中将生成[Cr(OH)4]-,[Cr(0H)4]-的结构可用示意图表示为
 .(不考虑空间构型)
.(不考虑空间构型)
分析 (1)Cr原子核外有24个电子,根据构造原理书写其核外电子排布式;
(2)单键都为σ键,双键中有1个σ键;
(3)乙醛中甲基上的C采取sp3杂化类型,醛基中的C采取sp2杂化类型;
(4)氢键的存在导致物质的熔沸点升高,乙醇分子间存在氢键,而乙醛分子间不存在氢键;
(5)原子个数及价电子数相等的微粒是等电子体;
(6)[Cr(OH)4]2-中是Cr3+与4个OH-形成配位键
解答 解:(1)Cr原子核外有24个电子,根据构造原理知其核外电子排布式为:[Ar]3d54s1或1s22s22p63s23p63d54s1,
故答案为:[Ar]3d54s1或1s22s22p63s23p63d54s1;
(2)CH3COOH分子中含有3个碳氢键、1个碳碳键、2个碳氧键和1个氧氢键;1mol乙酸分子含有6molσ键,
故答案为:6;
(3)乙醛(CH3CHO)中甲基上的C形成4条σ键,无孤电子对,因此采取sp3杂化类型,醛基中的C形成3条σ键和1条π键,无孤电子对,采取sp2杂化类型,
故答案为:sp2,sp3;
(4)氢键的作用力大于范德华力,则分子间形成氢键的沸点较高,C2H5OH分子间存在氢键,而CH3CHO分子间不能形成氢键,所以乙醇的沸点比乙醛的高,
故答案为:乙醇分子间存在氢键,而乙醛分子间不存在氢键;
(5)SO42-中含有5个原子,其价电子数是32,与SO42-互为等电子体的阴离子为:PO43-、SiO44-,
故答案为:PO43-或SiO44-;
(6)[Cr(OH)4]2-中的Cr2+与4个OH-形成配位键,可表示为 ,
,
故答案为:
点评 本题综合考查物质的结构与性质知识,侧重于电子排布式、σ键、杂化类型、氢键、等电子体与配位键等知识,题目难度中等,注意把握杂化类型的判断方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.短周期元素W、X、Y、Z的原子序数依次增大,W与Y最外层电子数之和为X的最外层电子数的2倍,Z最外层电子数等于最内层电子数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体.下列说法正确的是( )
| A. | 离子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z) | |
| B. | Y的最高价氧化物对应水化物的酸性比W的强 | |
| C. | W的气态氢化物比X的稳定 | |
| D. | WX2与ZY2中的化学键类型相同 |
13.下列措施不利于改善环境质量的是( )
| A. | 在燃煤中添加石灰石以减少酸雨的发生 | |
| B. | 严格执行机动车尾气排放标准 | |
| C. | 将所有垃圾通过露天焚烧、深埋的方式进行处理 | |
| D. | 利用二氧化碳等原料合成聚碳酸酯可降解塑料代替聚乙烯 |
10.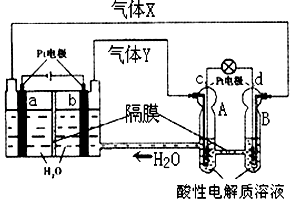 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )| A. | c极上进行还原反应,B中的H+可以通过隔膜进入A | |
| B. | d极上发生的电极反应是:O2+4H++4e-═2H2O | |
| C. | 该装置开始工作后,右端装置能量变化为:电能→化学能 | |
| D. | 当有0.2mol电子转移时,a极产生1.12L O2 |
17.造成大气污染的SO2主要来源于( )
| A. | 火山喷发 | |
| B. | 自然界中游离态硫缓慢氧化 | |
| C. | 煤、石油等含硫燃料的大量燃烧、硫矿石的冶炼及硫酸工业等产生的工业废气 | |
| D. | 汽车尾气 |
7.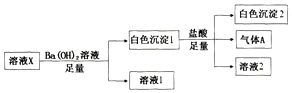 某溶液X中可能含有下列离子中的若干种:Cl-、SO42-、SO32-、HCO3-、Na+、Mg2+、Fe3+,所含离子的物质的量浓度均相同.为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如图实验:下列说法正确的是( )
某溶液X中可能含有下列离子中的若干种:Cl-、SO42-、SO32-、HCO3-、Na+、Mg2+、Fe3+,所含离子的物质的量浓度均相同.为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如图实验:下列说法正确的是( )
 某溶液X中可能含有下列离子中的若干种:Cl-、SO42-、SO32-、HCO3-、Na+、Mg2+、Fe3+,所含离子的物质的量浓度均相同.为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如图实验:下列说法正确的是( )
某溶液X中可能含有下列离子中的若干种:Cl-、SO42-、SO32-、HCO3-、Na+、Mg2+、Fe3+,所含离子的物质的量浓度均相同.为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如图实验:下列说法正确的是( )| A. | 气体A可能是CO2或SO2 | |
| B. | 溶液X中一定存在SO42-、HCO3-、Na+、Mg2+ | |
| C. | 溶液X中一定不存在Fe3+和Mg2+,可能存在Na+ | |
| D. | 分别在溶液1和溶液2中加入硝酸酸化的硝酸银溶液都能生成白色沉淀 |
14.下列实验操作能达到实验目的是( )
| 实验操作 | 实验目的 | |
| A | 将SO2通入紫色石蕊溶液中 | 证明SO2具有漂白性 |
| B | 取两支试管,分别加入4mlL0.01mol•L-1KMnO4溶液,然后向另一支试管中加入0.1mol•L-1H2C2O4溶液2mL,向另一支试管中加入0.1mol•L-1H2C2O4溶液4mL,记录褪色时间 | 证明草酸浓度越大,反应速率越快 |
| C | 向10mL0.2mol•L-1NaOH溶液中滴入2滴0.1mol•L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol•L-1FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的溶度积: Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| D | 向含酚酞的Na2SO3溶液中加入BaCl2溶液 | 证明Na2SO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
11.下列说法正确的是( )
| A. | 化合物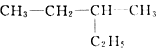 的名称是2-乙基丁烷 的名称是2-乙基丁烷 | |
| B. | 2-甲基丁烷和2,2-二甲基丙烷互为同系物 | |
| C. | 常温下,乙烯和苯都能被酸性KMnO4氧化,使KMnO4溶液褪色 | |
| D. | 等物质的量的乙烯和乙醇完全燃烧,消耗氧气的物质的量相等 |