题目内容
2.估计钙元素的电负性的取值范围( )| A. | 小于0.8 | B. | 大于1.2 | C. | 在0.8与1.2之间 | D. | 在0.8与1.5之间 |
分析 由表中数据可知,同一周期从左至右电负性增大,而同族元素从上到下元素电负性减小.
解答 解:由表中数据可知,同一周期从左至右电负性增大,而同族元素从上到下元素电负性减小,钙元素的电负性应小于Mg的而大于K的,即Ca的电负性的取值范围:0.8<X<1.2,
故选:C.
点评 本题考查电负性递变规律,侧重考查学生对数据的分析处理与归纳总结能力,注意对元素周期律的理解掌握.

练习册系列答案
相关题目
12.汽车尾气中含有CO、NO等有害气体.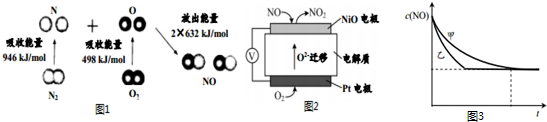
(1)汽车尾气中NO生成过程的能量变化示意图如图1.该条件下,1molN2和1molO2完全反应生成NO,会吸收(填“吸收”或“放出”)180kJ能量.
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图2所示:
①NiO电极上发生的是氧化反应(填“氧化”或“还原”).
②外电路中,电子流动方向是从NiO电极流向pt电极(填“NiO”或“pt”).
③pt电极上的电极反应式为O2+4e-=2O2-.
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO?2CO2+N2.已知增大催化剂的比表面积可提高该反应速率.为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中.
①请表中数据补充完整:a1.2×10-3;b5.80×10-3.
②能验证温度对化学反应速率规律的是实验Ⅰ和Ⅲ(填实验序号).
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图3所示,其中表示实验Ⅱ的是曲线乙(填“甲”或“乙”).

(1)汽车尾气中NO生成过程的能量变化示意图如图1.该条件下,1molN2和1molO2完全反应生成NO,会吸收(填“吸收”或“放出”)180kJ能量.
(2)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图2所示:
①NiO电极上发生的是氧化反应(填“氧化”或“还原”).
②外电路中,电子流动方向是从NiO电极流向pt电极(填“NiO”或“pt”).
③pt电极上的电极反应式为O2+4e-=2O2-.
(2)一种新型催化剂能使NO和CO发生反应:2NO+2CO?2CO2+N2.已知增大催化剂的比表面积可提高该反应速率.为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中.
| 实验编号 | t (℃) | NO初始浓度 | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.2×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.2×10-3 | b | 124 |
| Ⅲ | 350 | a | 5.8×10-3 | 82 |
②能验证温度对化学反应速率规律的是实验Ⅰ和Ⅲ(填实验序号).
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图3所示,其中表示实验Ⅱ的是曲线乙(填“甲”或“乙”).
13.在气体反应中,能使反应物中活化分子数和活化分子百分数同时增大的方法是( )
①移去生成物②升高温度③增大压强④增大反应物的浓度⑤加入催化剂.
①移去生成物②升高温度③增大压强④增大反应物的浓度⑤加入催化剂.
| A. | ①②③④⑤ | B. | ②③④⑤ | C. | ②⑤ | D. | ③④ |
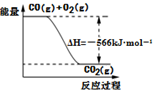
17.下列说法中正确的是( )

| A. | 6.8 g固体KHSO4与3.9 g固体Na2O2中阴离子数目相同 | |
| B. | 常温下铁、铜均不溶于浓硫酸,说明常温下铁、铜与浓硫酸均不反应 | |
| C. | 离子化合物中只含离子键 | |
| D. | 已知:2CO(g)+O2(g)═2CO2(g);△H=-566 kJ•mol-1,如图可表示由CO生成CO2的反应过程和能量关系 |
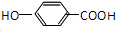
7.催化氧化的产物是 的醇是( )
的醇是( )
 的醇是( )
的醇是( )| A. |  | B. |  | ||
| C. |  | D. |  |
14.下列有关实验的操作正确的是( )
| A. | 检验某补铁药片(主要成分为亚铁化合物)是否氧化变质,使用氯水和硫氰化钾溶液 | |
| B. | 测定溶液pH时,可用pH试纸蘸取少量待测液,并与标准比色卡比较 | |
| C. | 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度,使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| D. | 测定碳酸钠中碳酸氢钠的含量:取a克样品与足量稀盐酸充分反应,逸出的气体通过碱石灰后,碱石灰增重b克,根据a和b的值即可求得碳酸氢钠的含量 |
9.某同学用中和滴定法测定某烧碱的纯度,实验过程如下:
(1)配制待测液
称取4.1g固体烧碱样品(杂质不与酸反应)配制成250mL溶液,需要的主要仪器有:托盘天平、烧杯、玻璃棒、250mL容量瓶、胶头滴管.
(2)滴定
①用碱式滴定管量取10.00mL待测液.
②向锥形瓶中加入几滴酚酞,用0.2010mol•L-1标准盐酸滴定待测烧碱溶液,边滴边摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,直到溶液由红色变为无色,且半分钟内不恢复时停止滴定.
(3)数据处理
根据上述各数据,计算待测烧碱溶液的浓度为0.4020mol•L-1,烧碱(40g/mol)的纯度为98.05%.
(4)下列操作,会导致实验结果偏低的是①②⑥(填序号);若把待测烧碱溶液放在滴定管中,则会导致实验结果偏低的是①④.
①碱式滴定管用蒸馏水洗净后没有用待测液润洗
②终点读数时俯视(滴定前读数准确)
③锥形瓶用蒸馏水洗净后没有用待测液润洗
④酸式 管尖端气泡没有排除,滴定后消失
⑤酸式滴定管用蒸馏水洗净后没有用标准液润洗
⑥振荡时锥形瓶中液滴飞溅出来.
(1)配制待测液
称取4.1g固体烧碱样品(杂质不与酸反应)配制成250mL溶液,需要的主要仪器有:托盘天平、烧杯、玻璃棒、250mL容量瓶、胶头滴管.
(2)滴定
①用碱式滴定管量取10.00mL待测液.
②向锥形瓶中加入几滴酚酞,用0.2010mol•L-1标准盐酸滴定待测烧碱溶液,边滴边摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,直到溶液由红色变为无色,且半分钟内不恢复时停止滴定.
(3)数据处理
| 实验次数编号 | 盐酸溶液体积V(mL) | 氢氧化钠溶液体积V(mL) |
| 1 | 19.90 | 10.00 |
| 2 | 20.10 | 10.00 |
| 3 | 22.00 | 10.00 |
| 4 | 20.00 | 10.00 |
(4)下列操作,会导致实验结果偏低的是①②⑥(填序号);若把待测烧碱溶液放在滴定管中,则会导致实验结果偏低的是①④.
①碱式滴定管用蒸馏水洗净后没有用待测液润洗
②终点读数时俯视(滴定前读数准确)
③锥形瓶用蒸馏水洗净后没有用待测液润洗
④酸式 管尖端气泡没有排除,滴定后消失
⑤酸式滴定管用蒸馏水洗净后没有用标准液润洗
⑥振荡时锥形瓶中液滴飞溅出来.
 .
. .
.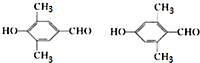 .
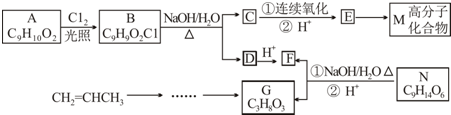
.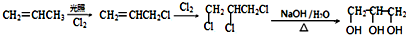 . (已知:CH2=CHCH3$→_{Cl_{2}}^{光照}$CH2=CHCH2Cl)
. (已知:CH2=CHCH3$→_{Cl_{2}}^{光照}$CH2=CHCH2Cl)