题目内容
17.硼酸(H3BO3)大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能,提高机械强度,缩短熔融时间.(1)H3BO3中B的化合价为+3.
(2)已知H3BO3与足量NaOH溶液反应的离子方程式为H3BO3+OH-═B(OH)4-,写出硼酸的电离方程式:H3BO3+H2O?B(OH)4-+H+.
分析 (1)根据化合物中各元素化合价代数和为0计算;
(2)由信息可知为一元酸,H3BO3电离除生成B(OH)4-外还生成H+.
解答 解:(1)在化合物中,氢元素显+1价,氧元素显-2价,根据化合物中各元素正负化合价的代数和为零原则,设B元素的化合价为x,则
(+1)×3+x+(-2)×3=0
x=+3,故答案为:+3;
(2)硼酸电离出四羟基和硼酸根和氢离子,方程式为:H3BO3+H2O?B(OH)4-+H+,
故答案为:H3BO3+H2O?B(OH)4-+H+.
点评 本题考查了化合物中元素化合价判断、电解质电离方程式的书写,明确化合物中各元素化合价代数和为0及电解质电离方式是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.25℃时,下列关于pH=2的醋酸溶液的叙述正确的是( )
| A. | 由水电离出的c(H+)=1.0×10-2mol•L-1 | |
| B. | 醋酸的电离平衡常数Ka=c(CH3COO-)•c(H+) | |
| C. | 若将溶液的温度升高到100℃,c(OH-)减小 | |
| D. | 加水稀释后H+的物质的量增加 |
12.用Cu2O可制备环保防污涂料.有一种制备Cu2O的方法是向CuSO4溶液中加入Na2SO3,加热,保持微沸一段时间,过滤得到Cu2O固体.已知:Cu2O+2H+→Cu+Cu2++H2O.下列说法正确的是( )
| A. | 反应过程的离子方程式:2Cu2++3SO32-→Cu2O↓+SO42-+2SO2↑ | |
| B. | 反应过程的离子方程式:2Cu2++3SO32-+2H2O→Cu2O↓+SO42-+4H+ | |
| C. | 加入过量Na2SO3有利于控制溶液的pH | |
| D. | 在酸性条件下,若有14.4g Cu2O变质,转移电子0.02mol |
5.北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).丙烷脱氢可得丙烯.
已知:C3H8(g)═CH4(g)+C2H2(g)+H2(g)△H1=+156.6kJ•mol-1
C3H6 (g)═CH4(g)+C2H2(g)△H2=+32.4kJ•mol-1
则相同条件下,反应C3H8(g)═C3H6 (g)+H2(g) 的△H 正确是( )
已知:C3H8(g)═CH4(g)+C2H2(g)+H2(g)△H1=+156.6kJ•mol-1
C3H6 (g)═CH4(g)+C2H2(g)△H2=+32.4kJ•mol-1
则相同条件下,反应C3H8(g)═C3H6 (g)+H2(g) 的△H 正确是( )
| A. | △H=一124.2kJ•mol-1 | B. | △H=+124.2kJ•mol-1 | ||
| C. | △H=+248.4kJ•mol-1 | D. | 不能确定 |
12.在粗盐提纯的实验中,操作正确的是( )
| A. | 把浑浊的液体倒入蒸发皿中加热 | |
| B. | 开始析出晶体后用玻璃棒搅拌 | |
| C. | 待水分完全蒸干后停止加热 | |
| D. | 蒸干水分后用玻璃棒转移固体至滤纸上 |
9.下列有关说法中正确的是( )
| A. | 向鸡蛋清溶液中加入饱和(NH4)2SO4溶液,有白色沉淀产生,说明蛋白质发生变性 | |
| B. | 苯中含有少量的苯酚可先加适量的浓溴水,使之生成2,4,6三溴苯酚,再过滤除去 | |
| C. | 用溴水检验CH2═CH-CHO中是否含有碳碳双键 | |
| D. | 麦芽糖及其水解产物均能发生银镜反应 |
10.X、Y、Z、M、R、Q为原子序数依次增大的六种短周期元素,其原子半径及主要化合价如下表:( )
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径/(×10-10m) | 0.37 | 0.75 | 0.74 | 1.86 | 1.43 | 0.99 | |
| 主要化合价 | 最高正价 | +1 | +5 | +1 | +3 | +7 | |
| 最低负价 | -1 | -3 | -2 | -1 | |||
| A. | Z的氢化物的稳定性都大于Y的氢化物 | |
| B. | 化合物XQ、MQ都是电解质,熔融状态下都能电解 | |
| C. | 元素M、Q、Z的简单离子半径:r(M+)>r(Q-)>r(Z2-) | |
| D. | 在一定条件下,R可以溶于M、Y两种元素的最高价氧化物的水化物的浓溶液 |
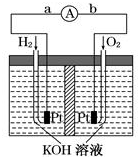 氢氧燃料电池是符合绿色化学理念的新型发电装置,图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置,图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答: