题目内容
5.北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).丙烷脱氢可得丙烯.已知:C3H8(g)═CH4(g)+C2H2(g)+H2(g)△H1=+156.6kJ•mol-1
C3H6 (g)═CH4(g)+C2H2(g)△H2=+32.4kJ•mol-1
则相同条件下,反应C3H8(g)═C3H6 (g)+H2(g) 的△H 正确是( )
| A. | △H=一124.2kJ•mol-1 | B. | △H=+124.2kJ•mol-1 | ||
| C. | △H=+248.4kJ•mol-1 | D. | 不能确定 |
分析 根据盖斯定律,由已知热化学方程式乘以合适的系数进行加减构造目标目标热化学方程式,反应热也乘以相应的系数,进行相应的加减,据此计算;
解答 解:已知:①C3H8(g)═CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ•mol-1
②CH3CH=CH2(g)═CH4(g)+HC≡CH(g )△H2=32.4kJ•mol-1
根据盖斯定律,①-②得C3H8(g)═CH3CH=CH2(g)+H2(g),
所以△H=△H1-△H2=156.6kJ•mol-1-32.4kJ•mol-1=+124.2kJ•mol-1,
故选B.
点评 本题考查反应热的计算,涉及盖斯定律的运用,注意目标热化学方程式的构建,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.锌锰干电池是家庭常用的电池,该电池工作时发生的化学反应为Zn+2NH4Cl+2MnO2═Zn(NH3)2Cl2+2MnO(OH),下列说法正确的是( )
| A. | 电池工作时锌片作为正极 | |
| B. | 电池工作时从负极向外电路输出电子 | |
| C. | 电池工作时MnO2发生还原反应 | |
| D. | 电池工作时电能向化学能转化 |
13.雾霾天气是一种大气污染状态,其污染的来源多种多样,如汽车尾气、工业排放、建筑扬尘、垃圾焚烧等.
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化.
①已知部分化学键的键能如下
请完成汽车尾气净化中发生反应的热化学方程式
2NO(g)+2CO(g)?N2(g)+2CO2(g) Q=-538KJ
②若上述反应在恒温、恒容的密闭体系中进行,t1时刻达到平衡状态,则下列示意图不符合题意的是ABC(填选项序号).
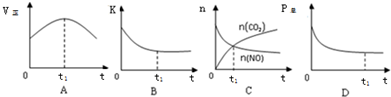
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.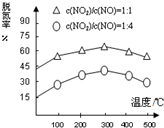
在氨气足量的情况下,不同c(NO2)/c(NO),不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请回答:温度对脱氮率的影响300℃之前,温度升高脱氮率逐渐增大,而300℃之后,温度升高脱氮率逐渐减小.
NH4Al (SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
(3)NH4Al(SO4)2可作净水剂,其理由是Al3+水解生成的Al(OH)3具有吸附性,即Al3++3H2O═Al(OH)3+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水.(用必要的方程式说明);相同条件下,0.1mol•L-1 NH4HSO4中c(NH4+)>(填“=”、“>”或“<”)0.1mol•L-1NH4Al(SO4)2中c(NH4+).

(4)如图1是0.1mol•L-1电解质溶液的pH随温度变化的图象.①其中符合0.1mol•L-1NH4Al(SO4)2的pH随温度变化的曲线是A(填写字母);
(5)室温时,向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示.试分析图中a、b、c、d四个点,水的电离程度最大的是a;在b点,溶液中各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化.
①已知部分化学键的键能如下
| 化学键 | N≡O | C≡O | C=O | N≡N |
| 键能(KJ/mol) | 632 | 1072 | 750 | 946 |
2NO(g)+2CO(g)?N2(g)+2CO2(g) Q=-538KJ
②若上述反应在恒温、恒容的密闭体系中进行,t1时刻达到平衡状态,则下列示意图不符合题意的是ABC(填选项序号).

(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.

在氨气足量的情况下,不同c(NO2)/c(NO),不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请回答:温度对脱氮率的影响300℃之前,温度升高脱氮率逐渐增大,而300℃之后,温度升高脱氮率逐渐减小.
NH4Al (SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
(3)NH4Al(SO4)2可作净水剂,其理由是Al3+水解生成的Al(OH)3具有吸附性,即Al3++3H2O═Al(OH)3+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水.(用必要的方程式说明);相同条件下,0.1mol•L-1 NH4HSO4中c(NH4+)>(填“=”、“>”或“<”)0.1mol•L-1NH4Al(SO4)2中c(NH4+).

(4)如图1是0.1mol•L-1电解质溶液的pH随温度变化的图象.①其中符合0.1mol•L-1NH4Al(SO4)2的pH随温度变化的曲线是A(填写字母);
(5)室温时,向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示.试分析图中a、b、c、d四个点,水的电离程度最大的是a;在b点,溶液中各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
10.物质的转化在给定条件下能实现的是( )
| A. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHCO3(s)$\stackrel{△}{→}$Na2CO3(s) | B. | CuCl2$\stackrel{NaOH(aq)}{→}$Cu(OH)2$→_{△}^{乙醛}$Cu | ||
| C. | Al$\stackrel{NaOH(aq)}{→}$NaAlO2(aq)$\stackrel{△}{→}$NaAlO2(s) | D. | Al2O3(s)$\stackrel{HCl(aq)}{→}$AlCl3(aq)$\stackrel{通电}{→}$Al(s) |
10.下列说法错误的是( )
| A. | ns电子的能量可能低于(n-1)p电子的能量 | |
| B. | 6C的电子排布式1s22s22px2反了洪特规则 | |
| C. | 电子排布式(21Sc)1s22s22p63s23p63d3违反了能量最低原理 | |
| D. | 电子排布式(22Ti)1s22s22p63s23p10违反了泡利原理 |
17.下列说法正确的是( )
| A. | 放热反应发生的过程中,只放出能量 | |
| B. | 化学反应中的能量通常表现为热量的变化 | |
| C. | 锌与盐酸反应是吸热的过程 | |
| D. | 反应物的总能量高于生成物的总能量为吸热反应 |
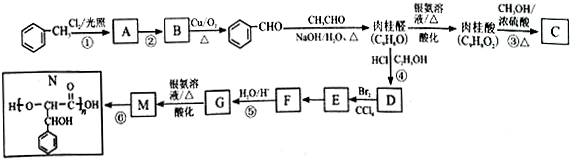
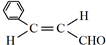 .
. .
. .
.