题目内容
17.如图是某同学设计的原电池装置,下列叙述中不正确的是( )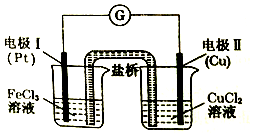
| A. | 盐桥中装有含氯化钾的琼脂,K+移向左池,Cl-移向右池 | |
| B. | 电极I上发生还原反应,电极反应式:Fe3++3e-=Fe | |
| C. | 电极Ⅱ作负极,铜电极逐渐溶解 | |
| D. | 该原电池的总反应为2 Fe3++Cu=Cu2++2Fe2+ |
分析 由图可知,负极发生Cu-2e-=Cu2+,正极发生Fe3++e-=Fe2+,总反应为2Fe3++Cu=Cu2++2Fe2+,阳离子向正极移动,阴离子向负极移动,以此来解答.
解答 解:A.I为正极,II负为极,盐桥中装有含氯化钾的琼脂,K+移向左池,Cl-移向右池,故A正确;
B.电极I为正极,发生还原反应,电极反应式为Fe3++e-=Fe2+,故B错误;
C.电极Ⅱ作负极,发生氧化反应,铜电极逐渐溶解,故C正确;
D.负极发生Fe3++e-=Fe2+,正极发生Cu-2e-=Cu2+,该原电池的总反应为2 Fe3++Cu=Cu2++2Fe2+,故D正确;
故选B.
点评 本题考查原电池,为高频考点,把握电极判断、电极反应、离子移动方向为解答的关键,侧重分析与应用能力的考查,注意原电池的工作原理,题目难度不大.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
7.下列说法正确的是( )
| A. | 在燃料改造过程中,“煤改气”发生物理变化,“煤改电”发生化学变化 | |
| B. | 硅胶和Na2SO4:10H2O可做袋装食品的干燥剂 | |
| C. | 亚硝酸盐有害身体健康,应禁止作为食品防腐剂 | |
| D. | “天宫”系列飞船使用的碳纤维材料是一种无机非金属材料 |
8.在溶液中进行的电离方程式的书写不正确的是( )
| A. | NH3•H2O?NH4++OH- | B. | CH3COOH?CH3COO-+H+ | ||
| C. | NaHCO3=Na++H++CO32- | D. | AlCl3=Al3++3Cl- |
5.在2A(g)+B(g)?3C(g)+4D(g)反应中,表示该反应速率最快的是( )
| A. | v(A)=1.2mol/(L•s) | B. | v(B)=0.5mol/(L•s) | C. | v(C)=1.5mol/(L•s) | D. | v(D)=2mol/(L•s) |
12.下列离子方程式表示正确的是( )
| A. | 硫化钠的水解反应:S2-+H3O+?HS-+H2O | |
| B. | 室温下,氯化铵溶液显酸性的理由:NH4++H2O═NH3•H2O+H+ | |
| C. | 泡沫灭火器的反应原理:Al3++3HCO3-═3CO2↑+Al(OH)3↓ | |
| D. | 用铜作电极电解饱和食盐水:2Cl-+H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- |
6.下列说法正确的是( )
| A. | 原电池的正极材料必须是金属 | |
| B. | 原电池的负极发生还原反应 | |
| C. | 实验室欲快速制取氢气,可利用粗锌与稀硫酸反应 | |
| D. | 原电池可以把物质内部的能量全部转化为电能 |
1.下列电离方程式错误的是( )
| A. | KClO3=K++Cl-+3O2- | B. | K2CO3=2K++CO32- | ||
| C. | NaOH=Na++OH- | D. | NH4Cl=NH4++Cl- |
