题目内容
6.下列说法正确的是( )| A. | 原电池的正极材料必须是金属 | |
| B. | 原电池的负极发生还原反应 | |
| C. | 实验室欲快速制取氢气,可利用粗锌与稀硫酸反应 | |
| D. | 原电池可以把物质内部的能量全部转化为电能 |
分析 A.燃料电池的电极材料为惰性电极;
B.负极发生氧化反应;
C.粗锌与稀硫酸可构成原电池反应;
D.原电池将化学能转化为电能,同时有热量产生.
解答 解:A.燃料电池的电极材料为惰性电极,则正极材料不一定是金属,故A错误;
B.负极失去电子,发生氧化反应,故B错误;
C.粗锌与稀硫酸可构成原电池反应,则可加快制取氢气的速率,故C正确;
D.原电池将化学能转化为电能,同时有热量产生,不能把物质内部的能量全部转化为电能,故D错误;
故选C.
点评 本题考查原电池,为高频考点,把握电池工作原理、电极反应为解答的关键,侧重分析与应用能力的考查,注意原电池的电极材料及能量转化,题目难度不大.

练习册系列答案
相关题目
17.如图是某同学设计的原电池装置,下列叙述中不正确的是( )
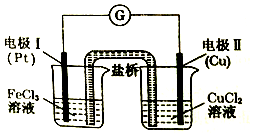

| A. | 盐桥中装有含氯化钾的琼脂,K+移向左池,Cl-移向右池 | |
| B. | 电极I上发生还原反应,电极反应式:Fe3++3e-=Fe | |
| C. | 电极Ⅱ作负极,铜电极逐渐溶解 | |
| D. | 该原电池的总反应为2 Fe3++Cu=Cu2++2Fe2+ |
14.下列离子方程式书写正确的( )
| A. | 沸水中滴入FeCl3饱和溶液:Fe3++3H2O$\frac{\underline{\;△\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | 氯气和水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 用氢氧化钠溶液吸收过量二氧化碳:OH-+CO2═HCO${\;}_{3}^{-}$ | |
| D. | Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
1.“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出 现甚至具有里程碑式划时代的意义.请回答下列问题:
Ⅰ、(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成 CaO•3MgO•4SiO2.
(2)高分子材料可以分成无机高分子材料和有机高分子材料.[AlFe(OH)n Cl6-n]m属于 无机高分子材料,是一种新型高效净水剂,它广泛应 用生活用水和工业污水的处 理,其中铁元素的化合价为+3;
Ⅱ、高纯二氧化硅可用来制造光纤.某稻壳灰的成分为:
通过如下流程可由稻壳灰制备较纯净的二氧化硅.
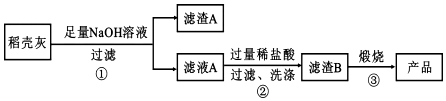
请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中属于两性氧化物的是Al2O3.
(2)步骤①中涉及 SiO2的离子反应方程式为SiO2+2OH-═SiO32-+H2O.
(3)滤渣 A 的成分有C和Fe2O3(填化学式)
Ⅰ、(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成 CaO•3MgO•4SiO2.
(2)高分子材料可以分成无机高分子材料和有机高分子材料.[AlFe(OH)n Cl6-n]m属于 无机高分子材料,是一种新型高效净水剂,它广泛应 用生活用水和工业污水的处 理,其中铁元素的化合价为+3;
Ⅱ、高纯二氧化硅可用来制造光纤.某稻壳灰的成分为:
| 组分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中属于两性氧化物的是Al2O3.
(2)步骤①中涉及 SiO2的离子反应方程式为SiO2+2OH-═SiO32-+H2O.
(3)滤渣 A 的成分有C和Fe2O3(填化学式)
11.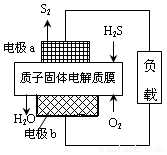 工业废气H2S经资源化利用后可回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.H2S燃料电池的工作原理如图所示.下列说法不正确的是( )
工业废气H2S经资源化利用后可回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.H2S燃料电池的工作原理如图所示.下列说法不正确的是( )
 工业废气H2S经资源化利用后可回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.H2S燃料电池的工作原理如图所示.下列说法不正确的是( )
工业废气H2S经资源化利用后可回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l)△H=-632kJ•mol-1.H2S燃料电池的工作原理如图所示.下列说法不正确的是( )| A. | 电极a为电池的正极 | |
| B. | 电极b上发生的电极反应为O2+4H++4e-=2H2O | |
| C. | 若电路中通过2mol电子,则电池内部释放632kJ热能 | |
| D. | 若有17gH2S参与反应,则会有1molH+经质子膜进入正极区 |
18.下列关于物质性质的表述正确的是( )
| A. | 向含有少量KSCN的FeI2溶液中滴加少量溴水,溶液出现血红色 | |
| B. | 用NH4HCO3固体以及其他固体药品能制得纯净的NH3 | |
| C. | 将SO2通入酸性KMnO4溶液中,溶液褪色,体现了SO2的漂白性 | |
| D. | 加热条件下,过量的Fe与浓硫酸反应只生成SO2一种气体 |
9.如图所示的实验操作正确的是( )
| A. |  点燃酒精灯 | B. |  称量10.05g固体 | C. |  液体加热 | D. |  量9.5mL液体 |
