题目内容
8.在溶液中进行的电离方程式的书写不正确的是( )| A. | NH3•H2O?NH4++OH- | B. | CH3COOH?CH3COO-+H+ | ||
| C. | NaHCO3=Na++H++CO32- | D. | AlCl3=Al3++3Cl- |
分析 A.一水合氨为弱电解质,部分电离出铵根离子和氢氧根离子;
B.醋酸是弱电解质,部分电离生成氢离子和醋酸根离子;
C.碳酸属于二元弱酸,碳酸氢钠为强电解质,完在水溶液中全电离生成钠离子与碳酸氢根离子;
D.AlCl3 在溶液中完全电离生成Al3+和Cl-离子.
解答 解:A.NH3•H2O为弱电解质,部分电离,电离方程式为:NH3•H2O?NH4++OH-,故A正确;
B.醋酸是弱电解质,部分电离,电离方程式为:CH3COOH?H++CH3COO-,故B正确;
C.碳酸氢钠为强电解质,完在水溶液中全电离生成钠离子与碳酸氢根离子,离子方程式为:NaHCO3=Na++HCO3-,故C错误;
D.氯化铝是强电解质,能完全电离出铝离子和氯离子,离子方程式为:AlCl3=Al3++3Cl-,故D正确;
故选C.
点评 本题考查了电解质电离方程式的书写,明确电解质的强弱是解题关键,注意弱电解质用可逆符号,强电解质用等号,注意弱酸的酸式根离子不能拆,题目难度不大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
18.下列说法正确的是( )
| A. | AlCl3溶液和Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同 | |
| B. | 配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度 | |
| C. | 向CuCl2溶液中加入CuO,调节溶液的pH可除去溶液中混有的Fe3+ | |
| D. | 泡沫灭火器中常使用的原料是碳酸钠和硫酸铝 |
19.下列离子方程式正确的是( )
| A. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | Fe2(SO4)3和Ba(OH)2溶液混合:2Fe3++3SO42-+3Ba2++6OH-═2Fe(OH)3↓+3BaSO4↓ | |
| C. | 硫酸工厂尾气中的SO2用过量的氨水吸收:2NH3•H2O+SO2═2NH4++SO32-+H2O | |
| D. | Cu溶于浓HNO3:Cu+4H++2NO3-═Cu2++2NO↑+4H2O |
3.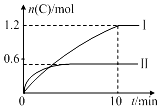 在2L的恒容密闭容器中充入A(g)和B(g),发生反应:A(g)+B(g)?2C(g)+D(s)△H=a kJ•mol-1实验内容和结果分别如表和图所示.下列说法正确的是( )
在2L的恒容密闭容器中充入A(g)和B(g),发生反应:A(g)+B(g)?2C(g)+D(s)△H=a kJ•mol-1实验内容和结果分别如表和图所示.下列说法正确的是( )
 在2L的恒容密闭容器中充入A(g)和B(g),发生反应:A(g)+B(g)?2C(g)+D(s)△H=a kJ•mol-1实验内容和结果分别如表和图所示.下列说法正确的是( )
在2L的恒容密闭容器中充入A(g)和B(g),发生反应:A(g)+B(g)?2C(g)+D(s)△H=a kJ•mol-1实验内容和结果分别如表和图所示.下列说法正确的是( )| 实验序号 | 温度 | 起始物质的量 | 热量变化 | |
| A | B | |||
| Ⅰ | 600℃ | 1 mol | 3 mol | 96 kJ |
| Ⅱ | 800℃ | 0.5 mol | 1.5 mol | -- |
| A. | a=160 | |
| B. | 600℃时,该反应的平衡常数是0.45 | |
| C. | 实验Ⅰ中,10 min内平均速率v(B)=0.06 mol•L-1•min-1 | |
| D. | 向实验Ⅱ的平衡体系中再充入0.5 mol A和1.5 mol B,A的转化率不变 |
13.化学与科学、技术、社会、环境密切相关.下列叙述不正确的是( )
| A. | 大气中PM2.5比表面积大,吸附力强,能吸附许多有毒、有害物质 | |
| B. | 氯气分别和氢氧化钠溶液、石灰乳反应得到的所有含氯化合物都具有漂白性 | |
| C. | 石墨烯是一种由单层碳原子构成的新纳米材料,具有导电性 | |
| D. | 刚玉、红宝石主要成分是氧化铝,陶瓷、分子筛主要成分是硅酸盐 |
20.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 34gH2O2中含有的阴离子数为1NA | |
| B. | 4.6g乙醇中含有的C-H键的个数为0.6NA | |
| C. | 标准状况下,VL水含有的氧原子个数约为$\frac{V}{22.4}$ | |
| D. | 1molFe2+与足量的H2O2溶液反应,转移NA个电子 |
17.如图是某同学设计的原电池装置,下列叙述中不正确的是( )
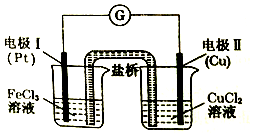

| A. | 盐桥中装有含氯化钾的琼脂,K+移向左池,Cl-移向右池 | |
| B. | 电极I上发生还原反应,电极反应式:Fe3++3e-=Fe | |
| C. | 电极Ⅱ作负极,铜电极逐渐溶解 | |
| D. | 该原电池的总反应为2 Fe3++Cu=Cu2++2Fe2+ |
18.下列关于物质性质的表述正确的是( )
| A. | 向含有少量KSCN的FeI2溶液中滴加少量溴水,溶液出现血红色 | |
| B. | 用NH4HCO3固体以及其他固体药品能制得纯净的NH3 | |
| C. | 将SO2通入酸性KMnO4溶液中,溶液褪色,体现了SO2的漂白性 | |
| D. | 加热条件下,过量的Fe与浓硫酸反应只生成SO2一种气体 |
