题目内容
16.某学生中和滴定实验的过程中如下:(a)取一支碱式滴定管;(b)用蒸馏水洗净;(c)即加入标准的NaOH溶液;(d)记录液面刻度读数;(e)用酸式滴定管精确放出一定量待测酸液;(f)置于未经待测酸液润洗的洁净锥形瓶中;(g)加入适量蒸馏水;(h)加入酚酞试液2滴;(i)滴定时,边滴边摇荡;(j)边注视滴定管内液面的变化;(k)当小心滴到溶液由无色变成粉红色时,即停止滴定;(l)记录液面刻度读数;(m)根据滴定管内的两次读数得出NaOH溶液体积为22mL.上述实验过程中的错误共几处( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
分析 滴定操作时,滴定管必须使用待装液润洗,锥形瓶不能润洗;滴定时眼睛应该注视锥形瓶中混合液颜色变化;滴定终点现象为溶液由无色变成粉红色且半分钟不褪色;滴定管读数应该读到0.01mL.
解答 解:c加入待测的NaOH溶液,碱式滴定管用蒸馏水洗完,必须使用待装液润洗,才能量取氢氧化钠溶液,故c错误;
j.边注视滴定管内液面变化,该操作错误,滴定时眼睛应该注视锥形瓶中溶液颜色变化,以便及时判断达到终点,故j错误;
k.当小心滴到溶液由无色变成粉红色且半分钟不褪色时,才能停止滴定,否则提前结束滴定,影响滴定结果,故k错误;
m.滴定管准确度为0.01mL,滴定管的两次读数得出NaOH溶液的体积应该为22.00mL,故m错误;
根据分析可知,错误的有4处,
故选C.
点评 本题考查化学实验方案的评价,主要考查中和滴定的操作、仪器、误差分析,题目难度不大,注意实验的基本操作方法及其规范性和注意事项,如:滴定时眼睛注视锥形瓶内液体颜色变化而不是滴定管内液面变化,为易错点.

练习册系列答案
相关题目
19.设阿伏加德罗常数的值为NA,则下列说法正确的是( )
| A. | 1.5g甲基所含有的电子数是NA | |
| B. | 28g乙烯所含共用电子对数目为6NA | |
| C. | 17g羟基所含有的电子数是10NA | |
| D. | 标准状况下,2.24 LCCl4中含Cl原子数目等于0.4NA |
1.已知Ba(AlO2)2可溶于水,下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述正确的是( )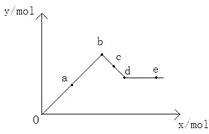

| A. | a-b时沉淀的物质的量:Al(OH)3比BaSO4多 | |
| B. | c-d时溶液中离子的物质的量:AlO2-比Ba2+多 | |
| C. | a-d时沉淀的物质的量:BaSO4可能小于Al(OH)3 | |
| D. | d-e时溶液中离子的物质的量:Ba2+可能等于OH- |
6.下列有关电解质溶液的说法正确的是( )
| A. | 常温下,0.1mol/LNa2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| B. | 0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:C(Na+)>c(CO32-)>c(HCO3- )>c(OH-)>c(H+) | |
| C. | pH相同的①CH3 COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ | |
| D. | 向0.1mol•L-1的氨水中加入少量硫酸铵固体,则溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 |