题目内容
已知:①向MnO2固体中加入浓盐酸,加热后充分反应,产生黄绿色气体,②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③向KMnO4晶体滴加浓盐酸,产生黄绿色气体.下列判断正确的为( )
| A、实验②证明Fe2+既有氧化性又有还原性 |
| B、实验③生成的气体不能使湿润的淀粉KI试纸变蓝 |
| C、上述实验中,有三个氧化还原反应 |
| D、上述实验证明氧化性:MnO2>MnO4->Cl2>Fe3+ |
考点:氧化还原反应
专题:氧化还原反应专题
分析:加热时MnO2能将浓盐酸氧化为氯气,MnO2做氧化剂,浓盐酸做还原剂;
KMnO4能氧化浓盐酸生成氯气;
氯气能将亚铁离子氧化为三价铁,氯气做氧化剂,亚铁离子做还原剂;
氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,
还原剂的还原性大于还原产物的还原性.
KMnO4能氧化浓盐酸生成氯气;
氯气能将亚铁离子氧化为三价铁,氯气做氧化剂,亚铁离子做还原剂;
氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,
还原剂的还原性大于还原产物的还原性.
解答:
解:A、②反应中Fe2+只是化合价升高,只具有还原性,故A错误;
B、实验③生成Cl2,氧化性强于I2,能使湿润的淀粉KI试纸变蓝,故B错误;
C、三个反应中都存在化合价的变化是氧化还原反应,故C正确;
D、高锰酸钾能将浓盐酸氧化为氯气,加热时MnO2能将浓盐酸氧化为氯气,则氧化性:MnO4->MnO2,MnO2做氧化剂,氯气是氧化产物,所以氧化性MnO2>Cl2,氯气能将亚铁离子氧化为三价铁,氯气做氧化剂,所以氧化性Cl2>Fe3+,则MnO4->MnO2>Cl2>Fe3,故D错误.
故选C.
B、实验③生成Cl2,氧化性强于I2,能使湿润的淀粉KI试纸变蓝,故B错误;
C、三个反应中都存在化合价的变化是氧化还原反应,故C正确;
D、高锰酸钾能将浓盐酸氧化为氯气,加热时MnO2能将浓盐酸氧化为氯气,则氧化性:MnO4->MnO2,MnO2做氧化剂,氯气是氧化产物,所以氧化性MnO2>Cl2,氯气能将亚铁离子氧化为三价铁,氯气做氧化剂,所以氧化性Cl2>Fe3+,则MnO4->MnO2>Cl2>Fe3,故D错误.
故选C.
点评:本题考查氧化还原反应,把握反应中元素的化合价变化是解答本题的关键,注意把握发生的两个反应,题目难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
下列各组离子能在同一溶液里大量共存的是( )
| A、Na+、Al3+、Cl-、AlO2- |
| B、Mg2+ NO3- Fe2+、H+ |
| C、Fe3+、SO42-、Na+、SCN- |
| D、K+、Na+、AlO2-、CO32- |
下列反应既是化合反应,又是氧化反应的是( )
A、2CO+O2
| ||||
| B、CaO+H2O=Ca(OH)2 | ||||
C、C+H2O
| ||||
| D、CO2+Ca(OH)2=CaCO3↓+H2O |
酸根RO3-所含电子数比硝酸根NO3-的电子数多10.则下列说法正确的是( )
| A、R原子的电子层数比N的电子层数多1 |
| B、R元素的最高正化合价与NO3-中的N的化合价相等 |
| C、RO3-和NO3-都只能被还原,不能被氧化 |
| D、R和N为同族元素 |
在光照条件下,将a mol甲烷与足量Cl2反应,测知四种产物的物质的量比依次2:1:1:2,则耗Cl2的物质的量为( )
| A、a mol |
| B、1.25a mol |
| C、2.5a mol |
| D、4a mol |
某无色溶液中可能含有I-、K+、Cu2+、SO32-(还原性:SO32->I-),向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是( )
①肯定不含I-; ②肯定不含Cu2+; ③肯定含有SO32-; ④可能含有I-.
①肯定不含I-; ②肯定不含Cu2+; ③肯定含有SO32-; ④可能含有I-.
| A、①③ | B、①②③ |
| C、②③④ | D、①② |
下列方程式书写正确的是( )
| A、醋酸的电离:CH3COOH+H2O?CH3COO-+H3O+ |
| B、H2SO3的电离方程式H2SO3?2H++SO32- |
| C、CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- |
| D、CaCO3的电离方程式:CaCO3?Ca2++CO32- |
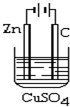 电解原理在工业有广泛的应用.利用相关知识回答下面的问题.
电解原理在工业有广泛的应用.利用相关知识回答下面的问题.