题目内容
9.下列不能根据元素电负性判断元素( )| A. | 是金属还是非金属 | B. | 正负化合价 | ||
| C. | 化学键类型 | D. | 化合物溶解度 |
分析 电负性是元素的原子在化合物中吸引电子能力的标度,电负性可以判断元素的金属性和非金属性,可以判断化合物中元素化合价的正负,可以判断化学键类型,以此来解答.
解答 解:A.电负性也可以作为判断元素的金属性和非金属性强弱的尺度.一般来说,电负性大于1.8的是非金属元素小于1.8的是金属元素,而位于非金属三角区边界的“类金属”(如锗、锑等)的电负性则在1.8左右,它们既有金属性又有非金属性,故A不选;
B.电负性能判断化合物中元素化合价的正负.电负性数值小的元素在化合物吸引电子的能力弱,元素的化合价为正值;电负性大的元素在化合物中吸引电子的能力强,元素的化合价为负值,故B不选;
C.电负性相同的非金属元素化合形成化合物时,形成非极性共价键;电负性差值小于1.7的两种元素的原子之间形成极性共价键,相应的化合物是共价化合物;电负性差值大于1.7的两种元素化合时,形成离子键,相应的化合物为离子化合物,故C不选;
D.电负性不能确定化合物的溶解度,故D选;
故选D.
点评 本题考查电负性及应用,为高频考点,把握电负性与非金属性的关系为解答的关键,侧重分析与应用能力的考查,注意电负性与溶解度无关,题目难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
20.将0.5mol下列物质分别加入100mL 5mol/L NaOH溶液中,完全反应后,所得溶液中阴离子浓度的大小顺序是( )
①Al ②Al2O3 ③Al(OH)3 ④AlCl3.
①Al ②Al2O3 ③Al(OH)3 ④AlCl3.
| A. | ①>②>③>④ | B. | ④>①>②>③ | C. | ②>①=③>④ | D. | ①>②=③>④ |
4. 如图所示,室温下,A、B两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下K夹,使两烧瓶内气体充分接触后,容器内压强由小到大的顺序正确的是( )
如图所示,室温下,A、B两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下K夹,使两烧瓶内气体充分接触后,容器内压强由小到大的顺序正确的是( )
 如图所示,室温下,A、B两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下K夹,使两烧瓶内气体充分接触后,容器内压强由小到大的顺序正确的是( )
如图所示,室温下,A、B两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下K夹,使两烧瓶内气体充分接触后,容器内压强由小到大的顺序正确的是( )| 编 号 | ① | ② | ③ | ④ |
| A中气体 | H2S | H2 | NH3 | NO |
| B中气体 | SO2 | Cl2 | HCl | O2 |
| A. | ②③④① | B. | ③①④② | C. | ③②①④ | D. | ④③②① |
14.下列分子或离子中不能与质子结合的是( )
| A. | F- | B. | H2O | C. | NH4+ | D. | NH3 |
1.城市饮用水的消毒剂有多种,液氯、漂白粉、二氧化氯、臭氧等,臭氧作为一种理想的消毒剂,杀菌能力强且不会影响水质,这是利用了臭氧的( )
| A. | 强还原性 | B. | 强氧化性 | C. | 助燃性 | D. | 不稳定性 |
18.下列有机物不能通过加成反应制取的是( )
| A. | CH3CH2Cl | B. | CH2Cl-CH2Cl | C. | CH3-CH2OH | D. | CH3 Cl |
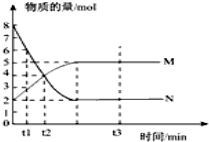 一定温度下,在容积为VL的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图示.
一定温度下,在容积为VL的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图示.