题目内容
3.下列说法正确的是( )| A. | 丙烷是直链烃,所以分子中3个碳原子也在一条直线上 | |
| B. | 丙烯所有原子均在同一平面上 | |
| C. | 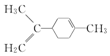 所有碳原子一定在同一平面上 所有碳原子一定在同一平面上 | |
| D. |  至少有16个原子共平面,至少8原子共线 至少有16个原子共平面,至少8原子共线 |
分析 A.直链烃是锯齿形的;
B.甲烷是正四面体结构;
C.因为环状结构不是平面结构;
D.苯环是平面结构,该分子中在同一条直线上的原子有8个.
解答 解:A.丙烷3个碳原子是锯齿形的,故A错误;
B.CH3-CH═CH2中甲基上至少有一个氢不和它们共平面,故B错误;
C.因为环状结构不是平面结构,所以所有碳原子不可能在同一平面上,故C错误;
D.该分子中在同一条直线上的原子有8个(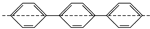 ),再加上其中一个苯环上的8个原子,所以至少有16个原子共平面,故D正确.
),再加上其中一个苯环上的8个原子,所以至少有16个原子共平面,故D正确.
故选D.
点评 本题主要考查有机化合物的结构特点,难度不大,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构.

练习册系列答案
相关题目
13.在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)?2SO3(g)△H=-Q kJ•mol-1(Q>0),某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )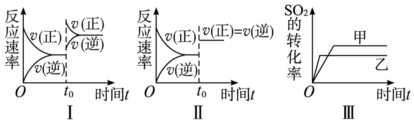

| A. | 图Ⅰ研究的是t0时刻增大O2的浓度对反应速率的影响 | |
| B. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较低 | |
| C. | 图Ⅲ研究的是催化剂对平衡的影响,且甲的催化效率比乙高 | |
| D. | 图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响 |
14.若1g CO2中含有x个原子,则阿伏加德罗常数可表示为( )
| A. | $\frac{1}{44}$ mol-1 | B. | $\frac{x}{22}$ mol-1 | C. | $\frac{3x}{44}$ mol-1 | D. | $\frac{44x}{3}$ mol-1 |
12.下列说法中不正确的是( )
| A. | 电解质不一定能导电 | |
| B. | 氨溶于水得到的氨水能导电,所以氨水是电解质 | |
| C. | 将硫酸钡放入水中不能导电,所以硫酸钡是非电解质 | |
| D. | 在水溶液或熔融状态下能导电的物质叫做电解质 |
16.铜及其化合物在工农业生产及日常生活中应用非常广泛.
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
①工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是反应不易控制,易还原产生Cu.
②已知:2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-169kJ•mol-1
C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5kJ•mol-1
Cu(s)+$\frac{1}{2}$O2(g)=CuO(s)△H=-157kJ•mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=+34.5kJ•mol-1.
(2)氢化亚铜是一种红色固体,可由下列反应制备
4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4
该反应每转移3mol电子,生成CuH的物质的量为1mol.
(3)氯化铜溶液中铜各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与c(Cl-) 的关系如图1.
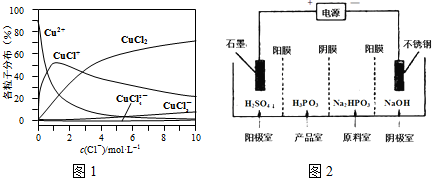
①当c(Cl-)=9mol•L-1时,溶液中主要的3种含铜物种浓度大小关系为c(CuCl2)>c(CuCl+)>c(CuCl3-).
②在c(Cl-)=1mol•L-1的氯化铜溶液中,滴入AgNO3溶液,含铜物种间转化的离子方程式为CuCl+═Cu2++Cl-(任写一个).
(4)已知:Cu(OH)2是二元弱碱;亚磷酸(H3PO3)是二元弱酸,与NaOH溶液反应,生成Na2HPO3.
①在铜盐溶液中Cu2+发生水解反应的平衡常数为5×10-9;(已知:25℃时,Ksp[Cu(OH)2]=2.0×10-20mol3/L3)
②电解Na2HPO3溶液可得到亚磷酸,装置如2图(说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过),则产品室中反应的离子方程式为HPO32-+2H+=H3PO3.
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法,反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑. |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
②已知:2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-169kJ•mol-1
C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5kJ•mol-1
Cu(s)+$\frac{1}{2}$O2(g)=CuO(s)△H=-157kJ•mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=+34.5kJ•mol-1.
(2)氢化亚铜是一种红色固体,可由下列反应制备
4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4
该反应每转移3mol电子,生成CuH的物质的量为1mol.
(3)氯化铜溶液中铜各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与c(Cl-) 的关系如图1.

①当c(Cl-)=9mol•L-1时,溶液中主要的3种含铜物种浓度大小关系为c(CuCl2)>c(CuCl+)>c(CuCl3-).
②在c(Cl-)=1mol•L-1的氯化铜溶液中,滴入AgNO3溶液,含铜物种间转化的离子方程式为CuCl+═Cu2++Cl-(任写一个).
(4)已知:Cu(OH)2是二元弱碱;亚磷酸(H3PO3)是二元弱酸,与NaOH溶液反应,生成Na2HPO3.
①在铜盐溶液中Cu2+发生水解反应的平衡常数为5×10-9;(已知:25℃时,Ksp[Cu(OH)2]=2.0×10-20mol3/L3)
②电解Na2HPO3溶液可得到亚磷酸,装置如2图(说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过),则产品室中反应的离子方程式为HPO32-+2H+=H3PO3.
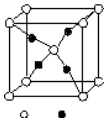 周期表前四周期的元素A、B、C、D、E,原子序数依次增大.A的核外电子总数与其周期数相同,B的价电子层中未成对电子有3个,C的最外层电子数为其内层电子数的3倍,D与C同族;E的最外层只有1个电子,但次外层有18个电子.回答下列问题;
周期表前四周期的元素A、B、C、D、E,原子序数依次增大.A的核外电子总数与其周期数相同,B的价电子层中未成对电子有3个,C的最外层电子数为其内层电子数的3倍,D与C同族;E的最外层只有1个电子,但次外层有18个电子.回答下列问题;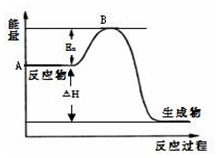 2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答:
2SO2(g)+O2(g)?2SO3(g)△H=a kJ•mol-1,反应过程的能量变化如图所示.已知1mol SO2(g)完全转化为1mol SO3(g)放热99kJ.请回答: