题目内容
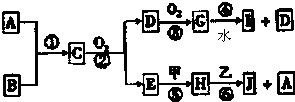
FeCl3溶液棕黄色,对此溶液,分别做如下实验,请填表:
| 编号 | 实践操作 | 实验主要现象 | 离子方程式 |
| ① | 加入过量 铁粉 | ||
| ② | 加入少量Na2O2粉末 | ||
| ③ | 加入少量AgNO3溶液 |
考点:铁盐和亚铁盐的相互转变
专题:元素及其化合物
分析:①氯化铁与铁发生氧化还原反应生成氯化亚铁,氯化亚铁为浅绿色;
②FeCl3溶液加入少量Na2O2粉末,过氧化钠先与水反应生成氢氧化钠和氧气,氢氧化钠与氯化铁发生复分解反应生成氢氧化铁和氯化钠,氢氧化铁为红褐色沉淀;
③氯化铁溶液加入硝酸银溶液,发生复分解生成氯化银沉淀,氯化银为白色沉淀.
②FeCl3溶液加入少量Na2O2粉末,过氧化钠先与水反应生成氢氧化钠和氧气,氢氧化钠与氯化铁发生复分解反应生成氢氧化铁和氯化钠,氢氧化铁为红褐色沉淀;
③氯化铁溶液加入硝酸银溶液,发生复分解生成氯化银沉淀,氯化银为白色沉淀.
解答:
解:①FeCl3溶液加入过量铁粉,离子反应的方程式为:2Fe3++Fe=3Fe2+,现象:铁粉部分溶解,溶液由棕黄色变浅绿色;
②FeCl3溶液加入少量Na2O2粉末,离子反应的方程式:2Na2O2+2H2O=4Na++4OH-+O2↑,Fe3++3OH-=Fe(OH)3↓,
反应生成红褐色沉淀放出气体;
③氯化铁溶液加入硝酸银溶液,离子方程式为:Ag++Cl-=AgCl↓,产生白色沉淀.
故答案为:
②FeCl3溶液加入少量Na2O2粉末,离子反应的方程式:2Na2O2+2H2O=4Na++4OH-+O2↑,Fe3++3OH-=Fe(OH)3↓,
反应生成红褐色沉淀放出气体;
③氯化铁溶液加入硝酸银溶液,离子方程式为:Ag++Cl-=AgCl↓,产生白色沉淀.
故答案为:
| 编号 | 实践操作 | 实验主要现象 | 离子方程式 |
| ① | 加入过量 铁粉 | 铁粉部分溶解,溶液由棕黄色变浅绿色 | 2Fe3++Fe=3Fe2+ |
| ② | 加入少量Na2O2粉末 | 反应生成红褐色沉淀放出气体 | 2Na2O2+2H2O=4Na++4OH-+O2↑ Fe3++3OH-=Fe(OH)3↓ |
| ③ | 加入少量AgNO3溶液 | 产生白色沉淀 | Ag++Cl-=AgCl↓ |
点评:本题考查了不同价态铁之间的转化,明确三价铁离子的性质,离子方程式的书写方法是解题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验方法能达到目的是( )
| A、用氨水清洗试管内壁附着的银镜 |
| B、用饱和Na2CO3溶液除去乙醇中少量的乙酸和水 |
| C、制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
| D、可用K3[Fe(CN)6]溶液鉴定FeCl3溶液中是否存在Fe2+ |
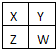 已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是( )
已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图所示,下列说法正确的是( )| A、若四种元素均为非金属,则W的最高价氧化物对应的水化物一定是强酸 |
| B、若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数) |
| C、若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱 |
| D、若四种元素中只有一种为金属,则Z与Y的最高价氧化物对应的水化物能反应 |
下列各组离子在相应的条件下一定能大量共存的是( )
| A、在碱性溶液中:HCO3-、K+、C1-、Na+ |
| B、与铝粉反应放出氢气的无色溶液中:NO3-、K+、Na+、SO42- |
| C、在c(H+)/c(OH-)═1×1013的溶液中:NH4+、Br-、C1-、K+ |
| D、通有SO2的溶液中:Ca2+、C1-、NO3-、A13+ |
 在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.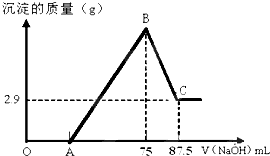 将一定量镁和铝的混合粉末加入50mL未知浓度的硫酸中,搅拌,得到澄清溶液.在此溶液中逐滴滴入8mol/L的NaOH溶液,滴加NaOH溶液的体积与产生沉淀的量如下图所示,请回答下列问题:
将一定量镁和铝的混合粉末加入50mL未知浓度的硫酸中,搅拌,得到澄清溶液.在此溶液中逐滴滴入8mol/L的NaOH溶液,滴加NaOH溶液的体积与产生沉淀的量如下图所示,请回答下列问题: