题目内容
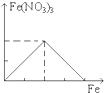
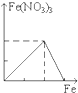
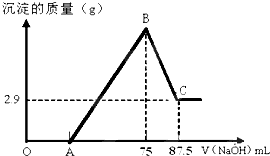 将一定量镁和铝的混合粉末加入50mL未知浓度的硫酸中,搅拌,得到澄清溶液.在此溶液中逐滴滴入8mol/L的NaOH溶液,滴加NaOH溶液的体积与产生沉淀的量如下图所示,请回答下列问题:
将一定量镁和铝的混合粉末加入50mL未知浓度的硫酸中,搅拌,得到澄清溶液.在此溶液中逐滴滴入8mol/L的NaOH溶液,滴加NaOH溶液的体积与产生沉淀的量如下图所示,请回答下列问题:(1)写出AB段的离子方程式
(2)2.9g沉淀的成分是
(3)计算所用硫酸的浓度
考点:铝的化学性质,镁的化学性质
专题:计算题
分析:由图可知,OA段发生H++OH-=H2O,继续滴加NaOH溶液,到沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液为硫酸钠溶液.再继续滴加NaOH溶液,到沉淀量开始进行,到沉淀量最小时,沉淀为Mg(OH)2,质量为2.9g,故到沉淀量最大,75mL~87.5mL发生Al(OH)3+NaOH=NaAlO2+2H2O,由元素守恒可知,n(Al)=n[Al(OH)3],n(Mg)=n[Mg(OH)2],再利用m=nM计算Al、Mg的质量.
解答:
解:由图可知,OA段发生H++OH-=H2O,继续滴加NaOH溶液,到沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液为硫酸钠溶液.再继续滴加NaOH溶液,到沉淀量开始进行,到沉淀量最小时,沉淀为Mg(OH)2,质量为2.9g,故到沉淀量最大,75mL~87.5mL发生Al(OH)3+NaOH=NaAlO2+2H2O,
(1)AB段的离子方程式为Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,故答案为:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓;
(2)2.9g沉淀的成分是Mg(OH)2,物质的量为
=0.05mol,Mg的质量为0.05mol×24g/mol=1.2g,75mL~87.5mL发生Al(OH)3+NaOH=NaAlO2+2H2O,n(Al)=n[Al(OH)3]=n(NaOH)=(87.5-75)×10-3L×8mol/L=0.1mol,Al的质量为0.1mol×27g/mol=2.7g,
故答案为:Mg(OH)2;1.2;2.7;
(3)B点溶液为硫酸钠溶液,n(硫酸)=2n(NaOH),则硫酸的浓度c=
=6mol/L,故答案为:6mol/L.
(1)AB段的离子方程式为Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,故答案为:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓;
(2)2.9g沉淀的成分是Mg(OH)2,物质的量为
| 2.9g |
| 58g/mol |
故答案为:Mg(OH)2;1.2;2.7;
(3)B点溶液为硫酸钠溶液,n(硫酸)=2n(NaOH),则硫酸的浓度c=
| 0.075L×8mol/L |
| 2×0.05L |
点评:本题考查镁铝化合物性质、混合物的计算,以图象题的形式考查,题目难度中等,分析图象各阶段的发生的反应是解题关键,侧重分析与计算能力的考查,注意守恒法在计算中应用.

练习册系列答案
相关题目
下列除去杂质所用的试剂和方法错误的是( )
| A、除去Na2CO3 固体中混有的少量的NaHCO3:置于坩埚中加热 |
| B、除去FeCl3酸性溶液中少量的FeCl2,加稍过量的双氧水后放置 |
| C、除去乙酸乙酯中混有的少量乙酸,加入乙醇并加热 |
| D、除去CO2中混有的少量的HC1:通过饱和的NaHCO3溶液中洗气 |
下列单质不能保存在煤油或石蜡油中的是( )
| A、K | B、Na | C、Ca | D、Li |