题目内容
化学方程式可简明地体现元素及其化合物的性质.已知氧化还原反应:
2FeCl3+2HI=2FeCl2+I2+2HCl;
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
2FeCl2+Cl2=2FeCl3
复分解反应:2CH3COOH+K2CO3=2CH3COOK+CO2↑+H2O;
KCN+CO2+H2O=HCN+KHCO3
热分解反应:4NaClO△3NaCl+NaClO4;
NaClO4△NaCl+2O2↑
下列说法不正确是( )
2FeCl3+2HI=2FeCl2+I2+2HCl;
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
2FeCl2+Cl2=2FeCl3
复分解反应:2CH3COOH+K2CO3=2CH3COOK+CO2↑+H2O;
KCN+CO2+H2O=HCN+KHCO3
热分解反应:4NaClO△3NaCl+NaClO4;
NaClO4△NaCl+2O2↑
下列说法不正确是( )
| A、还原性(酸性溶液):Fe2+>I->Cl- |
| B、氧化性(酸性溶液):Co(OH)3>Fe3+>I2 |
| C、酸性(水溶液):CH3COOH>H2CO3>HCN |
| D、热稳定性:NaCl>NaClO4>NaClO |
考点:氧化性、还原性强弱的比较
专题:氧化还原反应专题
分析:A、根据还原剂的还原性大于还原产物的还原性来判断;
B、根据氧化剂的氧化性大于氧化产物的氧化性判断;
C、根据化学反应遵循强酸制弱酸的规律来判断;
D、根据物质分解时生成更加稳定的物质来判断.
B、根据氧化剂的氧化性大于氧化产物的氧化性判断;
C、根据化学反应遵循强酸制弱酸的规律来判断;
D、根据物质分解时生成更加稳定的物质来判断.
解答:
解:A、在2FeCl3+2HI═2FeCl2+I2+2HCl反应中,还原性:HI>FeCl2,2FeCl2+Cl2=2FeCl3反应中,还原性:Fe2+>Cl-,故还原性应为:Fe2+>I->Cl-,故A错误;
B、在2FeCl3+2HI═2FeCl2+I2+2HCl反应中,氧化性:FeCl3>I2,在2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O中,氧化性:Co(OH)3>Cl2,2FeCl2+Cl2=2FeCl3反应中,氧化性:Cl2>FeCl3,则Co(OH)3>FeCl3,则有:Co(OH)3>FeCl3>I2,故B正确;
C、化学反应遵循强酸制弱酸的规律,在反应2CH3COOH+K2CO3═2CH3COOK+CO2↑+H2O中,酸性CH3COOH>H2CO3,在反应中KCN+CO2+H2O═HCN+KHCO3,酸性H2CO3>HCN,则酸性为CH3COOH>H2CO3>HCN,故C正确;
D、物质分解时生成更加稳定的物质,在反应中4NaClO
3NaCl+NaClO4,稳定性NaClO4>NaClO,在反应中NaClO4
NaCl+2O2↑中,稳定性NaCl>NaClO4,则稳定性NaCl>NaClO4>NaClO,故D正确;
故选A.
B、在2FeCl3+2HI═2FeCl2+I2+2HCl反应中,氧化性:FeCl3>I2,在2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O中,氧化性:Co(OH)3>Cl2,2FeCl2+Cl2=2FeCl3反应中,氧化性:Cl2>FeCl3,则Co(OH)3>FeCl3,则有:Co(OH)3>FeCl3>I2,故B正确;
C、化学反应遵循强酸制弱酸的规律,在反应2CH3COOH+K2CO3═2CH3COOK+CO2↑+H2O中,酸性CH3COOH>H2CO3,在反应中KCN+CO2+H2O═HCN+KHCO3,酸性H2CO3>HCN,则酸性为CH3COOH>H2CO3>HCN,故C正确;
D、物质分解时生成更加稳定的物质,在反应中4NaClO
| ||
| ||
故选A.
点评:本题考查氧化性、还原性、稳定性和酸性的比较,做题时注意积累比较物质的性质的规律和方法,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
白蚁分泌的蚁酸的化学性质与盐酸相似,能腐蚀很多建筑材料.下列材料中最不容易被白蚁蛀蚀的是( )
| A、钢 | B、铜 | C、大理石 | D、生铁 |
下列化学用语表达正确的是( )
A、NH4Cl的电子式: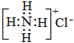 | ||
B、具有16个质子、16个中子和18个电子的微粒是
| ||
C、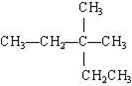 的名称为:2-甲基-2-乙基丁烷 的名称为:2-甲基-2-乙基丁烷 | ||
D、硝基苯的结构简式: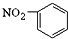 |
有一分子式为C8H14N2O3的二肽,经水解后得到丙氨酸CH3CH(NH2)COOH和另一种氨基酸R,则R的分子式为( )
| A、C3H7NO2 |
| B、C5H9NO2 |
| C、C5H9NO3 |
| D、C5H9NO4 |
下列说法不正确的是( )
①除去CO中混有的CO2,可让气体通过Na2O2粉末
②不慎将浓NaOH液沾在皮肤上,应立即用H2SO4溶液冲洗
③铝铁都能被冷的浓硫酸钝化,故铝铁和浓硫酸不反应
④做焰色反应实验时所用铂丝,每次用完后用稀硫酸洗涤后再使用.
①除去CO中混有的CO2,可让气体通过Na2O2粉末
②不慎将浓NaOH液沾在皮肤上,应立即用H2SO4溶液冲洗
③铝铁都能被冷的浓硫酸钝化,故铝铁和浓硫酸不反应
④做焰色反应实验时所用铂丝,每次用完后用稀硫酸洗涤后再使用.
| A、只有① | B、只有②③ |
| C、只有①③ | D、①②③④ |
反应3A(g)+B(g)=2C(g)+2D(g)在不同条件下反应,用不同物质表示的该反应速率分别为:
①υ(A)=0.8mol/L?min;
②υ(B)=0.45mol/L?min;
③υ(C)=0.015mol/L?s;
④υ(D)=0.45mol/L?min.
则在以上条件下,该反应速率的大小比较正确的是( )
①υ(A)=0.8mol/L?min;
②υ(B)=0.45mol/L?min;
③υ(C)=0.015mol/L?s;
④υ(D)=0.45mol/L?min.
则在以上条件下,该反应速率的大小比较正确的是( )
| A、①>②>③>④ |
| B、②=③>①>④ |
| C、②>①>④>③ |
| D、②>①=④>③ |
下列可证明甲烷分子是正四面体结构的是( )
| A、一氯甲烷没有同分异构体 |
| B、二氯甲烷没有同分异构体 |
| C、甲烷分子的四个键完全相同 |
| D、甲烷分子的四个键完全不相同 |
氢气与氮气的反应是一个释放能量的反应.在反应过程中,破坏1mo lH2 中的化学键吸收的能量为Q1 kJ,破坏1mol N2 中的化学键吸收的能量为Q2kJ,形成1mol NH3 中的化学键释放的能量为Q3 kJ.下列关系式中,正确的是( )
| A、3Q1+Q2<2Q3 |
| B、Q1+Q2>Q3 |
| C、3Q1+Q2>2Q3 |
| D、Q1+Q2<Q3 |