题目内容
下列化学用语表达正确的是( )
A、NH4Cl的电子式: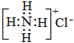 | ||
B、具有16个质子、16个中子和18个电子的微粒是
| ||
C、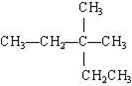 的名称为:2-甲基-2-乙基丁烷 的名称为:2-甲基-2-乙基丁烷 | ||
D、硝基苯的结构简式: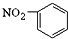 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氯离子电子式中,Cl满足8电子稳定结构;
B.16个质子、16个中子,其质量数为32,18个电子的微粒为硫离子;
C.主链含5个C,3号C上含2个甲基;
D.C与硝基中的N原子成键.
B.16个质子、16个中子,其质量数为32,18个电子的微粒为硫离子;
C.主链含5个C,3号C上含2个甲基;
D.C与硝基中的N原子成键.
解答:
解:A.NH4Cl的电子式为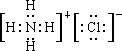 ,故A错误;
,故A错误;
B.16个质子、16个中子,其质量数为32,18个电子的微粒为硫离子,微粒是
S2-,故B正确;
C. 的名称为2,3-二甲基-戊烷,故C错误;
的名称为2,3-二甲基-戊烷,故C错误;
D.硝基苯的结构简式为 ,故D错误;
,故D错误;
故选B.
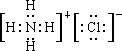 ,故A错误;
,故A错误;B.16个质子、16个中子,其质量数为32,18个电子的微粒为硫离子,微粒是
32 16 |
C.
 的名称为2,3-二甲基-戊烷,故C错误;
的名称为2,3-二甲基-戊烷,故C错误;D.硝基苯的结构简式为
 ,故D错误;
,故D错误;故选B.
点评:本题考查电子式、化学式及化学符号的综合应用,为高频考点,侧重化学用语使用的考查,注意化学用语的区别及规范应用为解答的关键,选项D为易错点,题目难度不大.

练习册系列答案
相关题目
在下列各组离子中,能大量共存的是( )
| A、Al3+、NH4+、AlO2-、Cl- |
| B、Cu2+、Fe2+、ClO-、SO42- |
| C、Na+、Ca2+、HCO3-、OH- |
| D、Cu2+、Fe3+、Cl-、NO3- |
50mL l8mol/L的硫酸与足量铜片共热,被还原的硫酸的物质的量是( )
| A、大于0.9 mol |
| B、等于0.45 mol |
| C、小于0.45mol |
| D、大于0.45 mol小于0.9 mol |
下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是( )
| A、氯气 | B、液氯 |
| C、新制氯水 | D、氯气的酒精溶液 |
下列有关高分子材料的表述不正确的是( )
| A、合成高分子材料都很难降解 |
| B、塑料、合成纤维、黏合剂、涂料等都是合成高分子材料 |
| C、棉花、羊毛、天然橡胶等属于天然高分子材料 |
| D、线型和体型高分子材料在溶解性、热塑性和热固性等方面有较大的区别 |
下列说法正确的是( )
| A、常温时,pH=12的溶液加水后,pH一定不小于7 |
| B、酸性氧化物加在水中,然后滴加紫色石蕊试液后一定呈红色 |
| C、打开汽水瓶盖有气泡逸出,此时饱和溶液变成了不饱和溶液 |
| D、非金属氧化物一定是酸性氧化物 |
能形成A2B型离子化合物的是( )
| A、原子序数为11和17的元素 |
| B、原子序数为12和9的元素 |
| C、原子序数为1和8的元素 |
| D、原子序数为11和16的元素 |
化学方程式可简明地体现元素及其化合物的性质.已知氧化还原反应:
2FeCl3+2HI=2FeCl2+I2+2HCl;
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
2FeCl2+Cl2=2FeCl3
复分解反应:2CH3COOH+K2CO3=2CH3COOK+CO2↑+H2O;
KCN+CO2+H2O=HCN+KHCO3
热分解反应:4NaClO△3NaCl+NaClO4;
NaClO4△NaCl+2O2↑
下列说法不正确是( )
2FeCl3+2HI=2FeCl2+I2+2HCl;
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
2FeCl2+Cl2=2FeCl3
复分解反应:2CH3COOH+K2CO3=2CH3COOK+CO2↑+H2O;
KCN+CO2+H2O=HCN+KHCO3
热分解反应:4NaClO△3NaCl+NaClO4;
NaClO4△NaCl+2O2↑
下列说法不正确是( )
| A、还原性(酸性溶液):Fe2+>I->Cl- |
| B、氧化性(酸性溶液):Co(OH)3>Fe3+>I2 |
| C、酸性(水溶液):CH3COOH>H2CO3>HCN |
| D、热稳定性:NaCl>NaClO4>NaClO |
海水是巨大的资源宝库,下列说法正确的是( )
| A、碘元素又称“海洋元素” |
| B、镁是海水中含量最多的金属元素 |
| C、从海水中提取食盐和碘的过程都是物理变化 |
| D、纯碱工业的原料有食盐 |