题目内容
 某课外小组利用如右图装置进行相关实验,请回答下列问题:
某课外小组利用如右图装置进行相关实验,请回答下列问题:(1)仪器D在实验中的作用是
(2)若将A容器中的液体逐滴加人到B容器的固体中,产生气体,该气体可以是(填化学式,写出2种即可)
(3)若 A中装有浓盐酸,B中装有高锰酸钾固体,C容器中装有淀粉碘化钾溶液,旋开E后,一段时间C中溶液变蓝色,写出B中发生反应的化学方程式
考点:常见气体制备原理及装置选择
专题:
分析:(1)依据仪器D装置的特点:干燥管下端刚没入液体内解答;为确保实验能够顺利进行,制取气体的装置要检查气密性;
(2)依据发生装置的特点:没有酒精灯,分液漏斗盛放液体,圆底烧瓶盛放液体或固体,结合常见气体反应原理解答;
(3)通过C容器中装有淀粉碘化钾溶液,旋开E后,一段时间C中溶液变蓝色,说明浓盐酸与高锰酸钾反应生成了氯气;浓盐酸在反应中既表现还原性又表现酸性,表现还原性的占参加反应盐酸的
,结合反应方程式计算氯气的体积.
(2)依据发生装置的特点:没有酒精灯,分液漏斗盛放液体,圆底烧瓶盛放液体或固体,结合常见气体反应原理解答;
(3)通过C容器中装有淀粉碘化钾溶液,旋开E后,一段时间C中溶液变蓝色,说明浓盐酸与高锰酸钾反应生成了氯气;浓盐酸在反应中既表现还原性又表现酸性,表现还原性的占参加反应盐酸的
| 10 |
| 16 |
解答:
解:(1)仪器D,干燥管下端刚没入液面以下,且干燥管中间容积较大,能很好的防治倒吸的发生,所以仪器D的作用是防止溶液倒吸;实验开始之前应进行的第一项操作是:检查整套装置气密性,故答案为:防止溶液倒吸;检查整套装置气密性;
(2)该装置可制取的气体的条件是反应物为固体和液体,反应条件不加热,实验室制备二氧化碳的原理:CaCO3+2 HCl=CaCl2+CO2↑+H2O,实验室制备氧气的反应原理:2H2O2
2H2O+O2↑,实验室制备氢气反应原理:Zn+H2SO4=H2↑+ZnSO4,所以可以制备的气体:CO2 H2 O2等;故答案为:CO2 H2 ;
(3)高锰酸钾与浓盐酸反应的化学方程式:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;
根据方程式可知当有2mol氯化氢被氧化时,生成1mol氯气,则当有1.6mol浓盐酸被氧化时,生成的氯气的物质的量为0.8mol,其体积为:0.8mol×22.4L/mol=17.92L,即17920mL,故答案为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;17920.
(2)该装置可制取的气体的条件是反应物为固体和液体,反应条件不加热,实验室制备二氧化碳的原理:CaCO3+2 HCl=CaCl2+CO2↑+H2O,实验室制备氧气的反应原理:2H2O2
| ||
(3)高锰酸钾与浓盐酸反应的化学方程式:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;
根据方程式可知当有2mol氯化氢被氧化时,生成1mol氯气,则当有1.6mol浓盐酸被氧化时,生成的氯气的物质的量为0.8mol,其体积为:0.8mol×22.4L/mol=17.92L,即17920mL,故答案为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;17920.
点评:本题考查了气体制备发生装置的选择,氯气的实验室和工业制法,题目难度中等,熟悉气体制备的反应原理是发生装置选择的关键,注意浓盐酸与高锰酸钾反应中表现的性质.

练习册系列答案
相关题目
下列关于实验的说法正确的是( )
| A、将二氧化碳通人硅酸钠溶液以证明碳酸的酸性比硅酸强 |
B、如图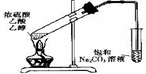 装置中,导管不能伸人液面的原因是产物易溶于水 装置中,导管不能伸人液面的原因是产物易溶于水 |
| C、用碱石灰可干燥氯气 |
| D、用普通玻璃棒蘸取溶液做焰色反应以证明溶液含有Na十 |
 某无色溶液中可能含有Mg2+、NH4+、K+、Al3+、SO42-、CO32-、Cl-等离子.现进行如下实验:①取10mL该溶液于试管中,滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到6.99g白色沉淀;②另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体(必要时可加热),最后沉淀完全溶解,并且随NaOH溶液的加入,沉淀和气体物质的量变化如图所示.下列说法不符合事实的是( )
某无色溶液中可能含有Mg2+、NH4+、K+、Al3+、SO42-、CO32-、Cl-等离子.现进行如下实验:①取10mL该溶液于试管中,滴加Ba(NO3)2溶液,加稀硝酸酸化后过滤得到6.99g白色沉淀;②另取10mL该溶液于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体(必要时可加热),最后沉淀完全溶解,并且随NaOH溶液的加入,沉淀和气体物质的量变化如图所示.下列说法不符合事实的是( )| A、根据图中数据计算实验中使用的NaOH溶液的浓度为1 mol?L-1 |
| B、根据信息分析该溶液中焰色反应呈紫色的离子的物质的量浓度为1 mol?L-1 |
| C、该溶液中NH4+、Al3+、SO42-三种离子的物质的量之比为2:1:3 |
| D、另取一定量该溶液滴加一定量Ba(OH)2溶液,不可能Al3+和SO42-同时完全沉淀 |
重铬酸钾为氧化剂,它与硫酸组成的铬酸洗液是实验室中常见的强氧化性洗液之一,其在实验室配制过程中产生大量的热.下列说法中,不正确的是( )
| A、配制前,用研钵把重铬酸钾研磨得越细越好 |
| B、把重铬酸钾粉末加到热水中,充分搅拌,使其溶解 |
| C、配制时,选用大容器的玻璃仪器(如 干燥器等) |
| D、在充分搅拌下把浓硫酸慢慢加入重铬酸钾溶液中 |
某烃与四倍于其体积的氧气混合,点燃后恢复到原来的温度和压强(1.01×106Pa、120℃)气体的体积不变.该烃是( )
| A、CH4 |
| B、C2H4 |
| C、C4H4 |
| D、C3H6 |
下列说法中,正确的是( )
| A、在紫外线、饱和(NH4)2SO4溶液、CuSO4溶液、福尔马林等作用下,蛋白质均会发生变性 |
| B、在一定条件下,氨基酸之间能发生反应,合成更复杂的化合物(多肽) |
| C、为检验皂化反应进行程度,取几滴反应液,滴入装有热水的试管中,震荡,若有油滴浮在液面上,说明油脂已完全反应 |
| D、检验淀粉在稀硫酸催化条件下水解产物的方法是:取适量水解液于试管中,加入少量新制Cu(OH)2悬浊液,加热煮沸,观察是否出现红色沉淀 |