题目内容
由白色和黑色固体组成的混合物A,可以发生如图1所示的一系列变化:

(1)写出反应③的化学方程式: .反应④的离子方程式: .
(2)操作②的名称是 .
(3)如图2,下列实验装置中可用于实验室制取气体G的发生装置的是 (填序号).为了得到纯净干燥的气体G,可将气体如图3通入装置a和b中,a、b两广口瓶中所装入的溶液依次是a: ,b: .
(4)气体G有毒,为了防止污染环境,必须将尾气进行处理,请写出d中发生反应的离子方程式: .
(5)J是一种极易溶于水的气体,为了防止倒吸,如图4下列e~i装置中,可用于吸收J的是 .


(1)写出反应③的化学方程式:
(2)操作②的名称是
(3)如图2,下列实验装置中可用于实验室制取气体G的发生装置的是
(4)气体G有毒,为了防止污染环境,必须将尾气进行处理,请写出d中发生反应的离子方程式:
(5)J是一种极易溶于水的气体,为了防止倒吸,如图4下列e~i装置中,可用于吸收J的是

考点:性质实验方案的设计
专题:实验设计题
分析:(1)G为黄绿色气体,则G为Cl2,反应③为二氧化锰与浓盐酸的反应生成氯化锰、氯气和水,方程式为MnO2+4HCl(浓)═Mn Cl2+Cl2+2H2O,则D为MnO2,所以C为MnO2、KCl的混合物则反应①为2KClO3
2KCl+3O2↑,A为KClO3、MnO2的混合物,气体B为O2,反应④的离子方程式:2Cl-+2H2O
Cl2+H2+2OH-;
(2)C为MnO2、KCl的混合物,KCl溶于水,而MnO2不溶于水,可利用溶解、过滤来分离;
(3)实验室制取氯气的反应为二氧化锰与浓盐酸加热生成,所以应选固液加热型的发生装置;根据制得的氯气中含有氯化氢和水蒸气杂质来选除杂试剂;
(4)氯气有毒,应连接氢氧化钠的尾气吸收装置;
(5)产生倒吸现象的原因就是一个:气体溶解或反应形成负压,将液体倒吸入前一个装置.
| ||
| △ |
| ||
(2)C为MnO2、KCl的混合物,KCl溶于水,而MnO2不溶于水,可利用溶解、过滤来分离;
(3)实验室制取氯气的反应为二氧化锰与浓盐酸加热生成,所以应选固液加热型的发生装置;根据制得的氯气中含有氯化氢和水蒸气杂质来选除杂试剂;
(4)氯气有毒,应连接氢氧化钠的尾气吸收装置;
(5)产生倒吸现象的原因就是一个:气体溶解或反应形成负压,将液体倒吸入前一个装置.
解答:
解:(1)G为黄绿色气体,则G为Cl2,反应③为二氧化锰与浓盐酸的反应生成氯化锰、氯气和水,方程式为MnO2+4HCl(浓)═Mn Cl2+Cl2+2H2O,则D为MnO2,所以C为MnO2、KCl的混合物则反应①为2KClO3
2KCl+3O2↑,A为KClO3、MnO2的混合物,气体B为O2,反应④的离子方程式:2Cl-+2H2O
Cl2+H2+2OH-,
故答案为:MnO2+4HCl(浓)═Mn Cl2+Cl2+2H2O;2Cl-+2H2O
Cl2+H2+2OH-;
(2)C为MnO2、KCl的混合物,KCl溶于水,而MnO2不溶于水,可利用过滤来分离,
故答案为:溶解、过滤;
(3)实验室制取氯气的反应为二氧化锰与浓盐酸加热生成,所以应选Ⅱ;要获得干燥纯净的黄绿色气体氯气,c装置中盛放饱和食盐水抑制氯气的溶解同时除去混有的HCl,d装置中盛放浓H2SO4干燥即可,故答案为:Ⅱ;饱和食盐水;浓H2SO4;
(4)氯气有毒,最后应连接用NaOH溶液吸收氯气的装置,反应的离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O,故答案为:2OH-+Cl2=Cl-+ClO-+H2O;
(5)可以在气体发生装置与气体装置间加一个平衡气压的装置,fhi均可起到防倒吸的作用,故答案为:fhi.
| ||
| △ |
| ||
故答案为:MnO2+4HCl(浓)═Mn Cl2+Cl2+2H2O;2Cl-+2H2O
| ||
(2)C为MnO2、KCl的混合物,KCl溶于水,而MnO2不溶于水,可利用过滤来分离,
故答案为:溶解、过滤;
(3)实验室制取氯气的反应为二氧化锰与浓盐酸加热生成,所以应选Ⅱ;要获得干燥纯净的黄绿色气体氯气,c装置中盛放饱和食盐水抑制氯气的溶解同时除去混有的HCl,d装置中盛放浓H2SO4干燥即可,故答案为:Ⅱ;饱和食盐水;浓H2SO4;
(4)氯气有毒,最后应连接用NaOH溶液吸收氯气的装置,反应的离子方程式为:2OH-+Cl2=Cl-+ClO-+H2O,故答案为:2OH-+Cl2=Cl-+ClO-+H2O;
(5)可以在气体发生装置与气体装置间加一个平衡气压的装置,fhi均可起到防倒吸的作用,故答案为:fhi.
点评:本题考查无机物的推断,利用物质的性质及发生的反应推断出各物质是解答本题的关键,题目难度不大,熟悉氧气的制法、氯气的制法及氯气的性质即可解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质属于天然高分子化合物的是( )
| A、油脂 | B、塑料 | C、淀粉 | D、葡萄糖 |
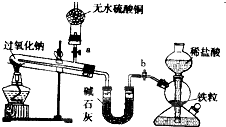 Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况下,设计了如图所示装置进行有关实验.
Na2O2是中学化学常用的强氧化剂,除了能与CO2、H2O反应外,还可与其他还原剂如H2、C发生反应,某化学课外兴趣小组为探究Na2O2与H2的反应情况下,设计了如图所示装置进行有关实验.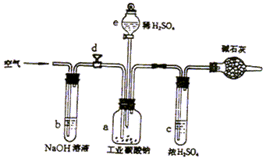 工业纯碱主要成份是无水碳酸钠,其中还含少量氯化钠,为测定工业纯碱中碳酸钠的质量分数:某学生设计了如图的装置:
工业纯碱主要成份是无水碳酸钠,其中还含少量氯化钠,为测定工业纯碱中碳酸钠的质量分数:某学生设计了如图的装置:
 50ml 0.5mol?L-1的盐酸与50ml 0.55mol?L-1的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.
50ml 0.5mol?L-1的盐酸与50ml 0.55mol?L-1的NaOH 溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.