题目内容
2.下列物质中,含非极性共价键的离子化合物的是( )| A. | MgCl2 | B. | Na2O2 | C. | NH3 | D. | NH4NO3 |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,不同非金属元素之间易形成极性键,同种非金属元素之间易形成非极性键,含有离子键的化合物为离子化合物,以此解答该题.
解答 解:A.氯化镁中只含离子键,为离子化合物,故A错误;
B.过氧化钠中钠离子和过氧根离子之间存在离子键、O原子之间存在非极性键,属于离子化合物,故B正确;
C.氨气为共价化合物,故C错误;
D.硝酸铵中存在离子键和极性键,故D错误.
故选B.
点评 本题考查离子键、极性键和非极性键,侧重考查基本概念,明确概念的内涵即可解答,会正确书写过氧化钠电子式,题目难度不大.

练习册系列答案
相关题目
17.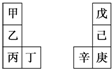 甲~辛等元素在周期表中的相对位置如表所示.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素.下列判断不正确的是( )
甲~辛等元素在周期表中的相对位置如表所示.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素.下列判断不正确的是( )
 甲~辛等元素在周期表中的相对位置如表所示.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素.下列判断不正确的是( )
甲~辛等元素在周期表中的相对位置如表所示.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素.下列判断不正确的是( )| A. | 金属性:甲>乙>丁 | |
| B. | 原子半径:辛>己>戊 | |
| C. | 丙和庚的原子核外电子数相差13 | |
| D. | 乙的单质在空气中燃烧生成离子化合物 |
7.下列实验的现象与对应结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显现象 | Al与浓硝酸不反应 |
| C | 向AlCl3溶液中滴加过量NaOH溶液 | 溶液澄清 | Al3+与NaOH能大量共存 |
| D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| A. | A | B. | B | C. | C | D. | D |
11.下列与实验相关的叙述正确的是( )
| A. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| B. | 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 | |
| C. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| D. | 取少量溶液依次加入BaCI2溶液和稀盐酸产生白色沉淀,则原溶液一定含有SO42- |
12.已知HF、CH3COOH均为弱酸,酸性强弱顺序为HF>CH3COOH,下列说法正确的是( )
| A. | 浓度均为0.1 mol•L-1的NaF、CH3COONa溶液相比较,CH3COONa溶液碱性较强 | |
| B. | 0.1 mol•L-1 CH3COOH溶液,加水稀释过程中,所有离子浓度均减小 | |
| C. | NaF溶液中只含有Na+、F-、H+、OH-、H2O五种微粒 | |
| D. | NaF溶液中加入少量NaOH固体,溶液中c(F-)变小 |
 mo1·L-1 B.
mo1·L-1 B. m
m ol·L-1
ol·L-1 mol·L-1 D.1000VMb(MV+2240) mol·L-1
mol·L-1 D.1000VMb(MV+2240) mol·L-1