题目内容
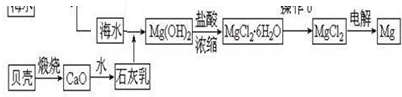
14.海洋是一个远未完全开发的巨大化学资源宝库,从海水中可得到多种化工原料和产品.Ⅰ.海水中含有氯化镁,是镁的重要来源之一.从海水中制取镁,某同学设计了如下流程步骤:
(1)写出向海水中加入石灰乳后发生反应的离子方程式:Mg2++Ca(OH)2=Mg(OH)2+Ca2+.
(2)下列说法不正确的是bc(填代号) a.此法的优点之一是原料来源丰富
b.电解MgCl2溶液制镁是由于镁是很活泼的金属
c.以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应.
Ⅱ.(1)铝、空气、海水可组成一种电池,广泛用于制造航标灯.此电池负极的电极反应为Al-3e-=Al3+.
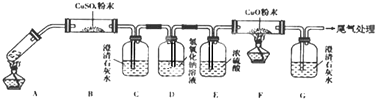
(2)铝热还原法是冶炼熔点较高的金属的一种重要方法,焊接钢轨即用到此法.将干燥的氧化铁粉末和铝粉均匀混合后放入纸漏斗中(漏斗已事先用水润湿),并架在铁架台上,下面放置一个盛有沙子的蒸发皿.请写出引发铝热反应的操作在铝热剂的上面加少量KClO3,中间插上镁条并将其点燃.
(3)为确定某铝热剂(氧化铁粉末和铝粉)中铝的质量分数,进行下列实验.
若取10.8g 样品,向其中加入足量的NaOH 溶液,测得生成的气体(标准状况)体积为3.36L,样品中铝的质量分数是25%.
分析 Ⅰ、海水加入石灰乳沉淀镁离子生成氢氧化镁沉淀,在盐酸溶液中浓缩蒸发得到结晶水合物,氯化氢气流中加热失去结晶水得到固体氯化镁,电解熔融氯化镁得到镁,
(1)向海水中加入石灰乳后反应生成氢氧化镁沉淀和氯化钙,石灰乳不能写成离子形式;
(2)从海水中制取镁主要存在以下的转化过程:MgCl2 $\stackrel{石灰乳}{→}$Mg(OH)2 $\stackrel{盐酸蒸发浓缩}{→}$MgCl2•6H2O$\stackrel{HCl气流中加热}{→}$MgCl2 $\frac{\underline{\;通电\;}}{\;}$Mg,利用此过程所涉及的反应和相关信息得出正确结论;
Ⅱ、(1)原电池工作时,铝为负极,被氧化,电极方程式为Al-3e-=Al3+;
(2)Fe2O3与Al粉混合物发生铝热反应,实质是置换反应,生成铁和氧化铝,引发铝热反应是用铝热剂的上面加少量KClO3,中间插上镁条并将其点燃,氧化铁和铝之间发生反应生成金属铁和氧化铝,反应的化学方程式为2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;
(3)铝和NaOH反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,n(H2)=0.15mol,根据化学方程式计算.
解答 解:Ⅰ、(1)向海水中加入石灰乳后反应生成氢氧化镁沉淀和氯化钙,石灰乳不能写成离子形式,反应的离子方程式为:Mg2++Ca(OH)2=Mg(OH)2+Ca2+,
故答案为:Mg2++Ca(OH)2=Mg(OH)2+Ca2+;
(2)a、原料来源于海水,故原料来源丰富,故a正确;
b、镁是很活泼的金属,可用电解熔融氯化镁的电解法制得,电解氯化镁溶液不能得到金属镁,故b错误;
c、①为分解反应和化合反应,②为复分解反应,③为复分解反应,④为分解反应,整个变化过程中无置换反应,故c错误,
故答案为:bc;
Ⅱ、(1)负极发生氧化反应,Al失去电子生成铝离子,电极反应式为:Al-3e-═Al3+,原电池工作时,电子从负极经外电路流向正极,
故答案为:Al-3e-=Al3+;
(2)Fe2O3与Al粉混合物发生铝热反应,实质是置换反应,生成铁和氧化铝,方程式为:2Al+Fe2O3═2Fe+Al2O3,引发铝热反应的实验操作是在铝热剂的上面加少量KClO3,中间插上镁条并将其点燃,
故答案为:在铝热剂的上面加少量KClO3,中间插上镁条并将其点燃;
(3)铝和NaOH反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,n(H2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2mol 3mol
n(Al) 0.15mol
n(Al)=0.1mol,
m(Al)=27g/mol×0.1mol=2.7g,
ω(Al)=$\frac{2.7g}{10.8g}$×100%=25%,
故答案为:25%.
点评 本题考查铝热反应以及化学方程式的计算,题目难度中等,本题注意铝热反应的原理,注意相关方程式的书写以及物质的量应用于化学方程式的计算方法.

 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 白磷分子的结构如图所示,小球表示磷原子,实线表示共价键,白磷分子中的每个P-P键之间插入一个氧原子后得化合物A,下列关于该化合物A的说法正确的是( )
白磷分子的结构如图所示,小球表示磷原子,实线表示共价键,白磷分子中的每个P-P键之间插入一个氧原子后得化合物A,下列关于该化合物A的说法正确的是( )| A. | 化合物A的分子式为P2O3 | |
| B. | 化合物A是磷酸的酸酐 | |
| C. | 化合物A是磷元素的最高价氧化物 | |
| D. | 化合物A中每个原子最外层都达到8电子的稳定结构 |
| A. | MgCl2 | B. | Na2O2 | C. | NH3 | D. | NH4NO3 |
| A. | N2分子中有一个σ键,2个π键 | |
| B. | 气体单质中,一定有σ键,可能有π键 | |
| C. | 通常,π键比σ键电子云重叠程度大,形成的共价键更牢固 | |
| D. | 两个原子间形成共价键时,σ键的数目取决于未成对电子的数目 |
 件下,等质量的H3和H2有相同的是( )
件下,等质量的H3和H2有相同的是( )