题目内容
19.“关爱生命,注意安全”.惨痛的天津爆炸触目惊心,火灾之后依然火势绵延不绝的原因之一是易燃物中含有电石.工业上常用电石(主要成分为CaC2,杂质为CaS等)与水反应生产乙炔气.(1)工业上合成CaC2主要采用氧热法.
已知:CaO(s)+3C(s)=CaC2(s)+CO(g)△H=+464.1kJ•mol-1
C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5kJ•mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO,为维持热平衡,每生产l molCaC2,转移电子的物质的量为10.4mol.
(2)已知2000℃时,合成碳化钙的过程中还可能涉及到如下反应
CaO(s)+C(s)=Ca(g)+CO(g) K1 △H1=a KJ•mol-1
Ca(g)+2C(s)=CaC2(s) K2 △H2=b KJ•mol-1
2CaO(s)+CaC2(s)=3Ca(g)+2CO(g) K3 △H3=c KJ•mol-1
则K1=$\sqrt{{K}_{2}{K}_{3}}$ (用含K2、K3的代数式表示);c=2a-b(用含a、b的代数式表示).
(3)利用电石产生乙炔气的过程中产生的H2S气体制取H2,既廉价又环保.

①利用硫化氢的热不稳定性制取氢气[2H2S(g)?S2(g)+2H2(g)].在体积为2L的恒容密闭容器中,H2S起始物质的量为2mol,达到平衡后H2S的转化率α随温度和压强变化如图l所示.据图计算T1℃、P1时平衡体系中H2的体积分数33.3%.由图知压强P1小于P2(填“大于”“小于”或“等于”),理由是相同温度下,压强增大,H2S分解反应逆向进行,所以P1小于P2.
②电化学法制取氢气的原理如图2,请写出反应池中发生反应的离子方程式H2S+S2O82-=S↓+2SO42-+2H+,惰性电极a上发生的电极反应式为2SO42--2e-=S2O82-.
分析 (1)若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO.则为了维持热平衡,所以每生产1molCaC2,则投料的量为:1molCaO、而投入碳的量为:3mol+$\frac{464.1kJ}{110.5kJ•mo{l}^{-1}}$=7.2mol,氧气的物质的量为$\frac{464.1kJ}{110.5kJ•mo{l}^{-1}}$×$\frac{1}{2}$=2.1mol,2.1mol氧气化合价降低8.4,1molCaC2化合物价降低2.0,共降低价数为10.4mol;
(2)由反应,①CaO(s)+C(s)?Ca(g)+CO(g)△H1=a kJ•mol-1;②Ca(g)+2C(s)?CaC2(s)△H2=b kJ•mol-1;根据盖斯定律,目标反应的反应热为:①×2-②得△H3=(2a-b)kJ•mol-1,K1=$\sqrt{K2K3}$;
(3)①根据三步法列出起始、变化和平衡时的物质的量,再根据气体的体积分数等于气体的物质的量分数计算;相同温度下,压强增大,H2S分解反应逆向进行,所以P1小于P2;
②反应池中H2S与S2O82-发生氧化还原反应;电解池中硫酸根离子失去电子,氢离子得到电子,以此来解答.
解答 解:(1)若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO.则为了维持热平衡,所以每生产1molCaC2,则投料的量为:1molCaO、而投入碳的量为:3mol+$\frac{464.1kJ}{110.5kJ•mo{l}^{-1}}$=7.2mol,氧气的物质的量为$\frac{464.1kJ}{110.5kJ•mo{l}^{-1}}$×$\frac{1}{2}$=2.1mol,2.1mol氧气化合价降低8.4,1molCaC2化合物价降低2.0,共降低价数为10.4mol,
故答案为:10.4;
(2)由反应,①CaO(s)+C(s)?Ca(g)+CO(g)△H1=a kJ•mol-1;②Ca(g)+2C(s)?CaC2(s)△H2=b kJ•mol-1;根据盖斯定律,目标反应=①×2-②,K1=$\sqrt{K2K3}$;反应热c=(2a-b)kJ•mol-1,
故答案为:$\sqrt{K2K3}$;(2a-b);
(3)①H2S起始浓物质的量为2mol,测定H2S的转化率,T1时H2S的转化率为40%,则
H2S(g)?H2(g)+1/2S2(g)
开始 2 0 0
转化0.8 0.8 0.4
平衡1.2 0.8 0.4
根据气体的体积分数等于气体的物质的量分数,P1时平衡体系中H2的体积分数=$\frac{0.8}{1.2+0.8+0.4}×100%$=33.3%;
相同温度下,压强增大,H2S分解反应逆向进行,所以P1小于P2;
故答案为:=33.3%;小于;相同温度下,压强增大,H2S分解反应逆向进行,所以P1小于P2;
②反应池中H2S与S2O82-发生氧化还原反应,离子方程式为H2S+S2O82-=S↓+2SO42-+2H+;电解池中硫酸根离子失去电子生成S2O82-,2SO42--2e-=S2O82-,
故答案为:H2S+S2O82-=S↓+2SO42-+2H+;2SO42--2e-=S2O82-.
点评 本题考查学生化学平衡常数、盖斯定律、化学平衡移动的影响和化学方程式的书写及计算方面的知识,综合性强,难度较大.

①NaOH ②NaHCO3③Al④苯⑤Na2SO4⑥NH3⑦HCl⑧甲烷.
| A. | ①②⑤⑥⑦ | B. | ①②③⑥⑦ | C. | ①④⑤⑥⑦ | D. | ①②⑥⑦⑧ |
| A. | 该溶液与K+、NO3-、OH-可以大量共存 | |
| B. | 该溶液显碱性的原因为ClO-+H2O?HClO+OH- | |
| C. | 向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| D. | 向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个 |
| A. | 羟基的电子式 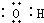 | B. | 丙烯的球棍模型 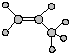 | ||
| C. | 乙炔的电子式  | D. | 乙酸的实验式 C2H4O2 |
| A. | Ba(OH)2溶液中加入过量Al2(SO4)3溶液:3Ba2++6OH-+2Al3++3SO42-═3 BaSO4↓+2Al(OH)3↓ | |
| B. | 将少量CO2通入NaClO溶液中:ClO-+CO2+H2O═HCO3-+HClO (已知:次氯酸的Ka为2.95×10-8,碳酸的Ka2为5.6×10-11) | |
| C. | 次氯酸钙溶液中通入足量SO2:Ca2++ClO-+SO2+H2O═CaSO4↓+Cl-+2H+ | |
| D. | 向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2HCO3-+2OH-═CO32-+CaCO3↓+2H2O |
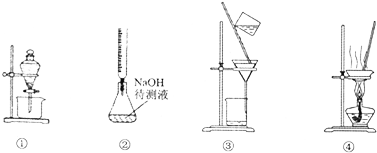
| A. | 图①表示分离CCl4和水的混合溶液的装置 | |
| B. | 图②表示已知浓度的盐酸溶液滴定未知浓度的氢氧化钠溶液的装置 | |
| C. | 图③表示分离二氧化锰和氯化锰溶液的装置 | |
| D. | 图④表示蒸干氯化铝溶液制AlCl3的装置 |