��Ŀ����
17����-���������ִ����ӹ�ҵ����;��Ϊ�㷺���ó�����ʯ����Fe2O3��FeO��Ҳ����Al2O3��MnO2��CuO�ȣ��Ʊ�������������ʵ���������£�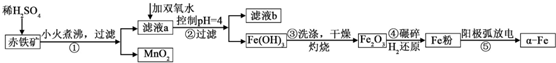
��֪������������������������ʽ��ȫ����ʱ��Һ��pH��
| ������ | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 |
��2�����ڢٲ��������õ�MnO2��KClO3��KOH��Һ���ȣ��ɵõ�K2MnO4���˷�Ӧ�Ļ�ѧ����ʽ��3MnO2+6KOH+KClO3=3 K2MnO4+KCl+3H2O��
��3���������������������оƾ��ơ����żܡ������ǡ�����������ǯ��
��4��������������õ绡����ʹ��������������������ʹ��������״�̻ҳ�����ΧX����ԭ�Ӽ�����ײ���г�ֵ����������͵�ɽ������ɦ�-Fe��X�������Ϊc��
a��O2b��N2c��Hed��H2
��5�������������ڿ�������ײ��ʱ��ȼ�գ��䷴Ӧ�����ڴ�����ȼ����ͬ��д���÷�Ӧ�Ļ�ѧ����ʽ3Fe+2O2$\frac{\underline{\;ײ��\;}}{\;}$Fe3O4��
���� Fe2O3��FeO��Al2O3��CuO�����ᷴӦ��a�н���������ΪCu2+��Al3+��Fe2+��Fe3+����˫��ˮ��Fe2+����ΪFe3+�����������ӳ���ʱpH���ݣ���֪����pH=4ʱ����������ȫ�����Fe��OH��3��������Һb����ҪΪCu2+��Al3+����������ϴ�Ӹ������յõ���������������������ԭ�õ��������ۣ����õ绡����ʹ��������������������ʹ��������״�̻ҳ�����Χ����Ӧ������ԭ�Ӽ�����ײ���г�ֵ����������͵�ɽ������ɦ�-Fe��
��1��pH��ֽ�ⶨ��ҺpH�IJ����ǰ�PH��ֽ���ڱ������ϣ��ò�����պȡ��Һ������ֽ�м䣬�۲���ɫ�仯�ͱ�ɫ�����ն�ȡ��ҺPH��
��2��MnO2��KClO3��KOH��Һ���ȣ�MnO2����ԭ��������K2MnO4��KClO3������������KCl��
��3�����չ�����ƾ��ơ����żܡ������ǡ�����������ǯ��
��4�����õ绡����ʹ��������������������ʹ��������״�̻ҳ�����ΧX����ԭ�Ӽ�����ײ���г�ֵ����������͵�ɽ������ɦ�-Fe��X�����������������͵�ɽ��������ò��ܺ���������Ӧ��
��5�������������ڿ�������ײ��ʱ��ȼ�գ��䷴Ӧ�����ڴ�����ȼ����ͬ��˵����������������������
��� �⣺��1�����������pH��ֽ�ⶨ��ҺpH�IJ����ǣ���һС��pH��ֽ���ڱ������ϣ��ò�����պȡ��������Һ������pH��ֽ�ϣ��������ɫ�����գ��������Һ�к��еĽ�����������Cu2+��Al3+�� ������������Ŀ��������Ӵ���������ԭ�ϵ�ת���ʺͷ�Ӧ���ʣ�
�ʴ�Ϊ����һС��pH��ֽ���ڱ������ϣ��ò�����պȡ��������Һ������pH��ֽ�ϣ��������ɫ�����գ� Cu2+��Al3+�� ����Ӵ���������ԭ�ϵ�ת���ʺͷ�Ӧ���ʣ�
��2�����ڢٲ��������õ�MnO2��KClO3��KOH��Һ���ȣ��ɵõ�K2MnO4��MnO2����ԭ��������K2MnO4��KClO3������������KCl���˷�Ӧ�Ļ�ѧ����ʽ�ǣ�
3MnO2+6KOH+KClO3=3 K2MnO4+KCl+3H2O��
�ʴ�Ϊ��3MnO2+6KOH+KClO3=3 K2MnO4+KCl+3H2O��
��3����������չ�������������оƾ��ơ����żܡ������ǡ�����������ǯ��
�ʴ�Ϊ�������ǡ�����������ǯ��
��4��������������õ绡����ʹ��������������������ʹ��������״�̻ҳ�����ΧX����ԭ�Ӽ�����ײ���г�ֵ����������͵�ɽ������ɦ�-Fe��X���岻�ܺ���������Ӧ������ΪHe��������Ϊa��O2��b��N2��d��H2����ѡc��
�ʴ�Ϊ��c��
��5�������������ڿ�������ײ��ʱ��ȼ�գ��䷴Ӧ�����ڴ�����ȼ����ͬ��˵������������������������Ӧ�Ļ�ѧ����ʽΪ��3Fe+2O2$\frac{\underline{\;ײ��\;}}{\;}$Fe3O4��
�ʴ�Ϊ��3Fe+2O2$\frac{\underline{\;ײ��\;}}{\;}$Fe3O4��
���� ���⿼�������ʷ��롢�����Ʊ���ʵ������������������ʵ�����Ӧ�õ�֪ʶ�㣬���ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д�| A�� | ͬ����Ԫ�ش��ϵ��£����ʵ��۵����� | |
| B�� | ͬ��������Ԫ�����Ӱ뾶���������μ�С | |
| C�� | HF��HCl��HBr��HI �����ȶ������μ�������ԭ�Ժ�ˮ��Һ������������ǿ | |
| D�� | �������ڷǽ���Ԫ�غ���������Դ�����������ǿ |
| A�� | KOH��aq��+$\frac{1}{2}$H2SO4��aq���T$\frac{1}{2}$K2SO4��aq��+H2O��l����H=-11.46 kJ•mol-1 | |
| B�� | 2KOH��aq��+H2SO4��aq���TK2SO4��aq��+2H2O��l����H=-11.46 kJ•mol-1 | |
| C�� | 2KOH��aq��+H2SO4��aq���TK2SO4��aq��+2H2O��l����H=+114.6 kJ•mol-1 | |
| D�� | KOH��aq��+$\frac{1}{2}$H2SO4��aq���T$\frac{1}{2}$K2SO4��aq��+H2O��l����H=-57.3 kJ•mol-1 |
| ʵ�� | ���� | |
| A | ��ȡ������������ | ����ڵ�����ˮ�а��ʵ������μ�FeCl3������Һ������������Һ��ʺ��ɫ��ֹͣ���� |
| B | ϡ��Ũ���� | �Ƚ�Ũ��������ձ��У���������ˮ |
| C | Ũ��ˮ����ʯ�ҷ�Ӧ�Ʊ������NH3 | �������ͨ��Ũ������������ſ������ռ� |
| D | �������������ͱ���̼������Һ | �ӷ�Һ©���Ͽڵ����л��㣬�ٴ��¿ڷų�ˮ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | ʯ���ѻ���ʯ�ͷ���ʯ���ѽ⡢ʯ�͵Ĵ��������ǻ�ѧ�仯 | |
| B�� | ����ʽΪC3H4Cl2���л����У�����ϩ������ͬ�����ŵĹ���5�� | |
| C�� | �ߴ��ȵľ��������Ʊ�����ܵȰ뵼�塢����оƬ���ά | |
| D�� | �ƾ���NaCl��Һ��CuSO4��Һ��ŨHNO3����ʹ�����ʷ������� |
| A�� | 66.6% | B�� | 42% | C�� | 50% | D�� | 33.3% |
| A�� | NH4Cl | B�� | Cu | C�� | SiO2 | D�� | I2 |