题目内容
某溶液中只可能含有K+、NO3-、SO42-、NH4+、CO32-中的几种(不考虑少量的H+与OH-),取200mL该溶液分成两等份,进行如下实验:一份加入足量烧碱并加热,产生气体在标准状况下为224mL;另一份先加足量盐酸无现象,再加入足量BaCl2得到2.33g固体,则该溶液中( )
| A、可能含有K+ |
| B、肯定含有NO3-、SO42-、NH4+、CO32- |
| C、一定不含有NO3- |
| D、一定含有K+ |
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:一份加入足量烧碱并加热,产生气体在标准状况下为224mL,说明原溶液中含有NH4+、且在一份样品中物质的量为0.01mol,另一份先加足量盐酸无现象,说明无CO32-,再加入足量BaCl2得到2.33g固体,说明有SO42-,且物质的量为0.01mol,据此答题.
解答:
解:一份加入足量烧碱并加热,产生气体在标准状况下为224mL,说明原溶液中含有NH4+、且在一份样品中物质的量为0.01mol,另一份先加足量盐酸无现象,说明无CO32-,再加入足量BaCl2得到2.33g固体,说明有SO42-,且物质的量为0.01mol,
A、因为在样品中NH4+为0.01mol,SO42-为0.01mol,根据电荷守恒,溶液中一定还有K+,故A错误;
B、加足量盐酸无现象,说明无CO32-,故B错误;
C、因为溶液中没有确定K+量是多少,所以也无法判断NO3-的有无,故C错误;
D、因为在样品中NH4+为0.01mol,SO42-为0.01mol,根据电荷守恒,溶液中一定还有K+,故D正确;
故选D.
A、因为在样品中NH4+为0.01mol,SO42-为0.01mol,根据电荷守恒,溶液中一定还有K+,故A错误;
B、加足量盐酸无现象,说明无CO32-,故B错误;
C、因为溶液中没有确定K+量是多少,所以也无法判断NO3-的有无,故C错误;
D、因为在样品中NH4+为0.01mol,SO42-为0.01mol,根据电荷守恒,溶液中一定还有K+,故D正确;
故选D.
点评:本题主要考查常见离子的检验,中等难度,解题的关键在于根据电荷守恒判断钾离子的存在.

练习册系列答案
相关题目
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
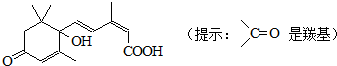
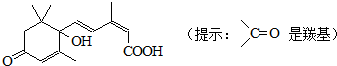
| A、含有羟基、羰基、羧基、酯基 |
| B、含有苯环、羟基、羰基、羧基 |
| C、含有碳碳双键、羟基、羰基、羧基 |
| D、含有碳碳双键、苯环、羟基、羰基 |
设NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A、1mol甲苯含有6NA个C-H键 |
| B、12 g石墨和C60的混合物中质子总数一定为6NA个 |
| C、25℃,pH=12的Na2CO3溶液中含有CO32-的数目为0.01NA |
| D、56g铁片投入足量浓硫酸中生成NA个SO2分子 |
 可逆反应A+aB?C+2D(a为化学计量数),已知B、C、D为气态物质.反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.下列说法不正确的是( )
可逆反应A+aB?C+2D(a为化学计量数),已知B、C、D为气态物质.反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.下列说法不正确的是( )| A、T2>T1,p2>p1 |
| B、该反应为放热反应 |
| C、若a=2,则A为液态或固态物质 |
| D、恒温恒容,增加B的物质的量,B的转化率增大 |
下列对于某些离子的检验说法中正确的是( )
| A、加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- |
| B、某溶液与NaOH溶液共热,产生使湿润蓝色石蕊试纸变红气体,说明原溶液中存在NH4+ |
| C、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| D、可用硝酸酸化的AgNO3溶液鉴别Cl-、Br-、I- |
一定质量的四种金属粉末,在足量的稀H2SO4中,生成标准状况下的氢气体积最大的是( )
| A、Na | B、Fe | C、Cu | D、Al |