题目内容
A、B、C、D、E、F均是元素周期表中按原子序数依次增大的前20号元素,其中只有A、D和B、E分别是同一主族元素,B、E两元素原子核中质子数之和是A、D两元素原子核中质子数之和的两倍,又知六种元素的单质中有三种气体、三种固体.部分元素在元素周期表中的相对位置关系如下:| C | |
| E |
(1)D、E组成的常见的化合物,其水溶液呈碱性,原因是______(用离子方程式表示).
(2)E的单质能跟D的最高价氧化物对应水化物的热浓溶液发生氧化还原反应,生成的两种正盐的水溶液均呈碱性,写出该氧化还原反应的离子方程式______.
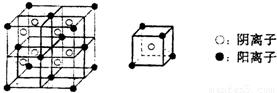
(3)C、F所形成的化合物为离子化合物,其晶体结构模型如下:该离子化合物的化学式为______.
(4)4.0gE的单质在足量的B的单质中完全燃烧,放出37.0kJ热量,写出其热化学方程式:______.
(5)用A元素的单质与B元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH浓溶液,两极均有特制的防止气体透过的隔膜,在A极通入A的单质,B极通入B的单质,则A极是该电池的______极;B极的电极反应式是______.
【答案】分析:A、B、C、D、E、F均是元素周期表中按原子序数依次增大的前20号元素,B、E是同一主族元素,B处于第二周期,E处于第三周期;A、D是同一主族元素,B、E两元素原子核中质子数之和是A、D两元素原子核中质子数之和的两倍,故A、D不可能分别处于第二周期、第三周期,也不可能分别处于第一周期、第二周期,不满足质子数故选,故A、D分别处于第一周期、第三周期,所以A为氢元素,D为钠元素;所以B、E两元素原子核中质子数之和为24,故B为氧元素,E为磷元素;结合C、E在周期表中的位置关系可知,C为反应元素;又知六种元素的单质中有三种气体、三种固体,F的原子序数等于磷元素,其中只有A、D和B、E分别是同一主族元素,故F为钙元素.
解答:解:A、B、C、D、E、F均是元素周期表中按原子序数依次增大的前20号元素,B、E是同一主族元素,B处于第二周期,E处于第三周期;A、D是同一主族元素,B、E两元素原子核中质子数之和是A、D两元素原子核中质子数之和的两倍,故A、D不可能分别处于第二周期、第三周期,也不可能分别处于第一周期、第二周期,不满足质子数故选,故A、D分别处于第一周期、第三周期,所以A为氢元素,D为钠元素;所以B、E两元素原子核中质子数之和为24,故B为氧元素,E为磷元素;结合C、E在周期表中的位置关系可知,C为反应元素;又知六种元素的单质中有三种气体、三种固体,F的原子序数等于磷元素,其中只有A、D和B、E分别是同一主族元素,故F为钙元素.
故A为氢元素,B为氧元素,C为氟元素,D为钠元素,E为硫元素,F为钙元素.
(1)D为钠元素,E为硫元素,二者组成常见化合物为Na2S,是强碱弱酸盐,S2-水解反应为S2-+H2O=HS-+OH-,使溶液呈碱性,故答案为:S2-+H2O=HS-+OH-;
(2)硫与氢氧化钠溶液发生反应,生成两种正盐的水溶液均呈碱性,该两种盐为硫化钠与亚硫酸钠,反应离子方程式为:3S+6OH-=2S2-+SO32-+3H2O,故答案为:3S+6OH-=2S2-+SO32-+3H2O;
(3)C为氟元素,F为钙元素,根据晶胞结构可知,Ca2+数目与F-数目之比为4× :1=1:2,所以化学式为CaF2,
:1=1:2,所以化学式为CaF2,
故答案为:CaF2;
(4)4.0g硫单质的物质的量为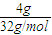 =
= mol,在足量的氧气中完全燃烧生成二氧化硫,放出37.0kJ热量,所以1mol硫,在足量的氧气中完全燃烧生成二氧化硫,放出296kJ热量,其热化学方程式:S(s)+O2(g)═SO2(g)△H=-296kJ/mol,故答案为:S(s)+O2(g)═SO2(g)△H=-296kJ/mol;
mol,在足量的氧气中完全燃烧生成二氧化硫,放出37.0kJ热量,所以1mol硫,在足量的氧气中完全燃烧生成二氧化硫,放出296kJ热量,其热化学方程式:S(s)+O2(g)═SO2(g)△H=-296kJ/mol,故答案为:S(s)+O2(g)═SO2(g)△H=-296kJ/mol;
(5)A为氢元素,B为氧元素,氢氧碱性燃料电池,电池总反应式均可表示为:2H2+O2=2H2O,负极发生氧化反应,在负极通入氢气,正极发生还原反应,在正极通入氧气;在A极通入A的单质,B极通入B的单质,则A极是该电池的负极;B极是电池的正极,氧气在此放电,电极反应式是O2+4e-+2H2O=4OH-,
故答案为:负;O2+4e-+2H2O=4OH-.
点评:本题考查元素周期表、结构与位置关系、热化学方程式、原电池、晶体结构等,难度中等,推断元素是解题的根据,突破口是B、E两元素原子核中质子数之和是A、D两元素原子核中质子数之和的两倍,据此确定A、D在周期表中的位置.
解答:解:A、B、C、D、E、F均是元素周期表中按原子序数依次增大的前20号元素,B、E是同一主族元素,B处于第二周期,E处于第三周期;A、D是同一主族元素,B、E两元素原子核中质子数之和是A、D两元素原子核中质子数之和的两倍,故A、D不可能分别处于第二周期、第三周期,也不可能分别处于第一周期、第二周期,不满足质子数故选,故A、D分别处于第一周期、第三周期,所以A为氢元素,D为钠元素;所以B、E两元素原子核中质子数之和为24,故B为氧元素,E为磷元素;结合C、E在周期表中的位置关系可知,C为反应元素;又知六种元素的单质中有三种气体、三种固体,F的原子序数等于磷元素,其中只有A、D和B、E分别是同一主族元素,故F为钙元素.
故A为氢元素,B为氧元素,C为氟元素,D为钠元素,E为硫元素,F为钙元素.
(1)D为钠元素,E为硫元素,二者组成常见化合物为Na2S,是强碱弱酸盐,S2-水解反应为S2-+H2O=HS-+OH-,使溶液呈碱性,故答案为:S2-+H2O=HS-+OH-;
(2)硫与氢氧化钠溶液发生反应,生成两种正盐的水溶液均呈碱性,该两种盐为硫化钠与亚硫酸钠,反应离子方程式为:3S+6OH-=2S2-+SO32-+3H2O,故答案为:3S+6OH-=2S2-+SO32-+3H2O;
(3)C为氟元素,F为钙元素,根据晶胞结构可知,Ca2+数目与F-数目之比为4×
 :1=1:2,所以化学式为CaF2,
:1=1:2,所以化学式为CaF2,故答案为:CaF2;
(4)4.0g硫单质的物质的量为
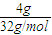 =
= mol,在足量的氧气中完全燃烧生成二氧化硫,放出37.0kJ热量,所以1mol硫,在足量的氧气中完全燃烧生成二氧化硫,放出296kJ热量,其热化学方程式:S(s)+O2(g)═SO2(g)△H=-296kJ/mol,故答案为:S(s)+O2(g)═SO2(g)△H=-296kJ/mol;
mol,在足量的氧气中完全燃烧生成二氧化硫,放出37.0kJ热量,所以1mol硫,在足量的氧气中完全燃烧生成二氧化硫,放出296kJ热量,其热化学方程式:S(s)+O2(g)═SO2(g)△H=-296kJ/mol,故答案为:S(s)+O2(g)═SO2(g)△H=-296kJ/mol;(5)A为氢元素,B为氧元素,氢氧碱性燃料电池,电池总反应式均可表示为:2H2+O2=2H2O,负极发生氧化反应,在负极通入氢气,正极发生还原反应,在正极通入氧气;在A极通入A的单质,B极通入B的单质,则A极是该电池的负极;B极是电池的正极,氧气在此放电,电极反应式是O2+4e-+2H2O=4OH-,
故答案为:负;O2+4e-+2H2O=4OH-.
点评:本题考查元素周期表、结构与位置关系、热化学方程式、原电池、晶体结构等,难度中等,推断元素是解题的根据,突破口是B、E两元素原子核中质子数之和是A、D两元素原子核中质子数之和的两倍,据此确定A、D在周期表中的位置.

练习册系列答案
相关题目
 [化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.
[化学/选修/物质结构与性质]A、B、C、D、E五种短周期元素,原子序数依次增大,各元素对应的单质均为固体.A、C、E三元素的原子核外均只有2个未成对电子.B、E元素的原子序数之和等于C、D元素的原子序数之和.