题目内容
3.设NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 1mol Cl2与足量Fe反应,转移的电子数为3NA | |
| B. | 1molNa2O2固体跟足量CO2气体完全反应,转移NA个电子 | |
| C. | 标准状况下,11.2LSO3所含的分子数为0.5NA | |
| D. | 100mL 0.1mol/L盐酸中含HCl分子数为0.01NA |
分析 A、氯气和铁反应后变为-1价;
B、过氧化钠与二氧化碳反应为歧化反应;
C、标况下三氧化硫为固体;
D、盐酸中无HCl分子.
解答 解:A、氯气和铁反应后变为-1价,故1mol氯气转移2mol电子即2NA个,故A错误;
B、过氧化钠与二氧化碳反应为歧化反应,故1mol过氧化钠转移1mol电子即NA个,故B正确;
C、标况下三氧化硫为固体,不能根据气体摩尔体积来计算其物质的量和分子个数,故C错误;
D、HCl在溶液中能完全电离,故盐酸中无HCl分子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
13.下列反应属于取代反应的是( )
| A. | 乙醇在浓硫酸作用下加热制乙烯 | B. | 石油裂解制丙烯 | ||
| C. | 苯和液溴反应制溴苯 | D. | 乙烯制聚乙烯 |
14.下列说法能用平衡移动原理解释的是( )
| A. | 在电解水实验中,加入硫酸钠可以提高电解效率 | |
| B. | 碳酸氢钠溶液与硫酸铝溶液混合有沉淀和气体生成 | |
| C. | 铁制品在海水中比在纯水中更易腐蚀 | |
| D. | 在双氧水中加FeCl3溶液可使产生O2速率加快 |
11.以石墨为电极,电解KI溶液(其中含有少量酚酞和淀粉).下列说法错误的是( )
| A. | 溶液的pH变小 | B. | 阴极逸出气体 | ||
| C. | 阳极附近溶液呈蓝色 | D. | 阴极附远溶液呈红色 |
8.下列实验过程中,始终无明显现象的是( )
| A. | Cl2通入NaHCO3溶液中 | B. | CO2通入CaCl2溶液中 | ||
| C. | NH3通入AlCl3溶液中 | D. | SO2通入Ba(NO3)2溶液中 |
15.对于某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 某溶液中加入硝酸银溶液,产生白色沉淀,该溶液中一定含有Cl- |
12.下面是四种元素的基态原子的电子排布式,其中化合价最高的是( )
| A. | 1s22s22p3 | B. | 1s22s22p63s23p63d34s2 | ||
| C. | 1s22s22p63s23p6 | D. | 1s22s22p5 |
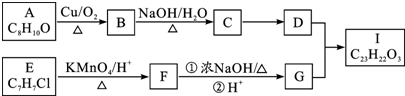
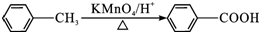
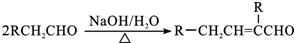
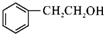 ,C→D的反应类型为加成反应,F中不含氧的官能团的名称为氯原子,I的结构简式为
,C→D的反应类型为加成反应,F中不含氧的官能团的名称为氯原子,I的结构简式为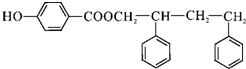 .
. ,F→G①的化学方程式为
,F→G①的化学方程式为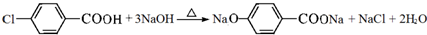 .
.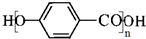 .
.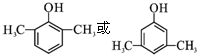 .
.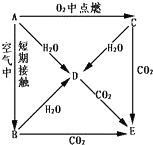 A、B、C、D、E五种物质都含钠元素,它们按图所示关系相互转化,已知A 为单质.
A、B、C、D、E五种物质都含钠元素,它们按图所示关系相互转化,已知A 为单质.