题目内容
Ⅰ.甲醇是一种重要的化工原料和新型燃料.
Ⅰ.工业上一般以CO和H2为原料在密闭容器中合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ?mol-1
在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律.如图1是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线Z对应的温度是 ;该温度下上述反应的化学平衡常数为 ;若增大H2的用量,上述反应的热效应最大值为 .
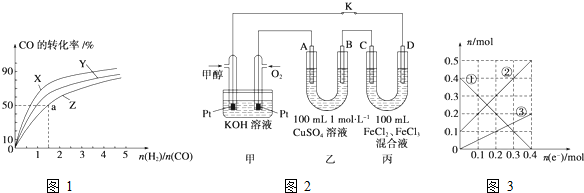
Ⅱ.如图2是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
(1)甲中负极的电极反应式为 .
(2)乙中A极析出的气体在标准状况下的体积为 .
(3)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图3,则图中②线表示的是 的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要 mL 5.0mol?L-1 NaOH溶液.
Ⅰ.工业上一般以CO和H2为原料在密闭容器中合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ?mol-1
在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律.如图1是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线Z对应的温度是

Ⅱ.如图2是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
(1)甲中负极的电极反应式为
(2)乙中A极析出的气体在标准状况下的体积为
(3)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图3,则图中②线表示的是
考点:转化率随温度、压强的变化曲线,常见化学电源的种类及其工作原理,化学平衡建立的过程,化学平衡的影响因素
专题:基本概念与基本理论
分析:Ⅰ.正反应放热,则升高温度CO的转化率降低;计算出平衡时各物质的浓度,结合平衡常数的定义进行计算;
Ⅱ.(1)通入甲醇的一极为原电池的负极,发生氧化反应,甲醇在碱性条件下被氧化生成碳酸根离子;
(2)工作一段时间后,断开K,此时A、B两极上产生的气体体积相同,分析电极反应,B为阴极,溶液中铜离子析出,氢离子得到电子生成氢气;A电极为阳极,溶液中的氢氧根离子失电子生成氧气;阳极电极反应和电子守恒计算得到;
(3)C电极为阳极,D电极为阴极,根据丙图可知溶液中有三种金属阳离子,而根据丙的成分可知溶液中只有两种金属阳离子,说明在电解过程中还有Cu2+生成,因此C电极是Cu做阳极,D电极是石墨做阴极,根据转移电子的物质的量和金属阳离子的物质的量的变化确定曲线对应的离子,结合转移电子的物质的量计算.
Ⅱ.(1)通入甲醇的一极为原电池的负极,发生氧化反应,甲醇在碱性条件下被氧化生成碳酸根离子;
(2)工作一段时间后,断开K,此时A、B两极上产生的气体体积相同,分析电极反应,B为阴极,溶液中铜离子析出,氢离子得到电子生成氢气;A电极为阳极,溶液中的氢氧根离子失电子生成氧气;阳极电极反应和电子守恒计算得到;
(3)C电极为阳极,D电极为阴极,根据丙图可知溶液中有三种金属阳离子,而根据丙的成分可知溶液中只有两种金属阳离子,说明在电解过程中还有Cu2+生成,因此C电极是Cu做阳极,D电极是石墨做阴极,根据转移电子的物质的量和金属阳离子的物质的量的变化确定曲线对应的离子,结合转移电子的物质的量计算.
解答:
解:Ⅰ.根据该反应为放热反应,温度越高CO的转化率越小,所以曲线Z为270℃,
由图象可知当270℃时,CO的转化率为50%,n(H2):n(CO)=1.5,则
CO(g)+2H2(g)?CH3OH (g)
起始(mol/L) 1 1.5 0
转化(mol/L) 0.5 1 0.5
平衡(mol/L) 0.5 0.5 0.5
K=
=
=4,
增大H2的用量,提高CO的转化率,当1molCO完全转化时,则放出90.8 kJ的热量,但该反应为可逆反应,故增大H2的用量,上述反应的热效应最大值接近90.8 kJ,
故答案为:270℃,4;90.8 kJ;
Ⅱ.(1)甲醇燃料电池是原电池反应,甲醇在负极失电子发生氧化反应,电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O,
故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;
(2)工作一段时间后,断开K,此时A、B两极上产生的气体体积相同,分析电极反应,B为阴极,溶液中铜离子析出,氢离子得到电子生成氢气,设生成气体物质的量为X,溶液中铜离子物质的量为0.1mol,电极反应为:
Cu2++2e-=Cu,
0.1mol 0.2mol
2H++2e-=H2↑,
2x x
A电极为阳极,溶液中的氢氧根离子失电子生成氧气,电极反应为:
4OH--4e-=2H2O+O2↑,
4x x
根据得失电子守恒得到0.2+2x=4x,
x=0.1mol
乙中A极析出的气体是氧气,物质的量为0.1mol,在标准状况下的体积为2.24L,
故答案为:2.24L;
(3)根据转移电子的物质的量和金属阳离子的物质的量的变化,可知,铜离子从无增多,铁离子物质的量减小,亚铁离子增加,故①为Fe3+,②为Fe2+,③为Cu2+,
由图可知电子转移为0.4mol,生成Cu2+物质的量为0.2mol,阴极电极反应Fe3++e-=Fe2+,反应结束后,溶液中有Fe2+为0.5mol,Cu2+为0.2mol,所以需要加入NaOH溶液0.5×2+0.2×2=1.4mol,所以所需NaOH溶液的体积为
=0.28L=280mL,
故答案为:Fe2+;280.
由图象可知当270℃时,CO的转化率为50%,n(H2):n(CO)=1.5,则
CO(g)+2H2(g)?CH3OH (g)
起始(mol/L) 1 1.5 0
转化(mol/L) 0.5 1 0.5
平衡(mol/L) 0.5 0.5 0.5
K=
| c(CH3OH) |
| c(CO)?c2(H2) |
| 0.5 |
| 0.5×0.5×0.5 |
增大H2的用量,提高CO的转化率,当1molCO完全转化时,则放出90.8 kJ的热量,但该反应为可逆反应,故增大H2的用量,上述反应的热效应最大值接近90.8 kJ,
故答案为:270℃,4;90.8 kJ;
Ⅱ.(1)甲醇燃料电池是原电池反应,甲醇在负极失电子发生氧化反应,电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O,
故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;
(2)工作一段时间后,断开K,此时A、B两极上产生的气体体积相同,分析电极反应,B为阴极,溶液中铜离子析出,氢离子得到电子生成氢气,设生成气体物质的量为X,溶液中铜离子物质的量为0.1mol,电极反应为:
Cu2++2e-=Cu,
0.1mol 0.2mol
2H++2e-=H2↑,
2x x
A电极为阳极,溶液中的氢氧根离子失电子生成氧气,电极反应为:
4OH--4e-=2H2O+O2↑,
4x x
根据得失电子守恒得到0.2+2x=4x,
x=0.1mol
乙中A极析出的气体是氧气,物质的量为0.1mol,在标准状况下的体积为2.24L,
故答案为:2.24L;
(3)根据转移电子的物质的量和金属阳离子的物质的量的变化,可知,铜离子从无增多,铁离子物质的量减小,亚铁离子增加,故①为Fe3+,②为Fe2+,③为Cu2+,
由图可知电子转移为0.4mol,生成Cu2+物质的量为0.2mol,阴极电极反应Fe3++e-=Fe2+,反应结束后,溶液中有Fe2+为0.5mol,Cu2+为0.2mol,所以需要加入NaOH溶液0.5×2+0.2×2=1.4mol,所以所需NaOH溶液的体积为
| 1.4 |
| 5 |
故答案为:Fe2+;280.
点评:本题综合性较大,涉及化学平衡常数、化学平衡影响因素以及电化学知识等,难度较大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下列叙述中正确的是( )
| A、金属钠在氯气中燃烧会产生棕黄色烟 |
| B、漂粉精在空气中容易失效的原因是次氯酸钙不稳定,易分解 |
| C、氯水经光照后产生的气体是挥发的氯气 |
| D、常温下1体积水中能溶解2体积Cl2,所以饱和氯水是稀溶液 |
关于12C、14C、13N、14N几种原子的相互关系描述正确的是( )
| A、14C和14N质量数相同,互为同位素 |
| B、12C和14N含有相同的中子数 |
| C、12C和13N中子数相同,质子数不同,互为同位素 |
| D、12CO和14CO物理性质不同,化学性质基本相同 |
下列有关物质的性质和该性质的应用均正确的是( )
| A、SiO2具有较好的导电性,可用于制造半导体材料 |
| B、H2O2是一种绿色氧化剂,可氧化酸性高锰酸钾而产生O2 |
| C、铜的金属活动性比铁弱,可用铜罐代替铁罐贮运浓硝酸 |
| D、Mg在空气中燃烧发出耀眼的白光,可用于制作信号弹 |

 工业上一般在密闭容器中采用下列反应合成甲醇:
工业上一般在密闭容器中采用下列反应合成甲醇: