题目内容
类推是化学学习和研究中常用的思维方法.下列类推错误的是( )
①Mg可由电解熔融MgCl2制取;则Al也可由电解熔融AlCl3制取
②晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子
③1mol?L-1的NaCl溶液每升中含有1mol Na+;则1mol?L-1的FeCl3溶液每升中也含有1mol Fe3+
④使用pH试纸时必须保持干燥;则湿润的pH试纸测得的pH一定有误差.
①Mg可由电解熔融MgCl2制取;则Al也可由电解熔融AlCl3制取
②晶体中有阴离子,必有阳离子;则晶体中有阳离子,也必有阴离子
③1mol?L-1的NaCl溶液每升中含有1mol Na+;则1mol?L-1的FeCl3溶液每升中也含有1mol Fe3+
④使用pH试纸时必须保持干燥;则湿润的pH试纸测得的pH一定有误差.
| A、①③ | B、①③④ |
| C、②③④ | D、①②③④ |
考点:金属冶炼的一般原理,金属晶体,测定溶液pH的方法,盐类水解的应用
专题:类比迁移思想
分析:①氯化铝是共价化合物,熔融物中不含自由移动的铝离子;
②在金属晶体中,存在金属阳离子和自由移动的电子;
③铁离子在溶液中要水解,但是钠离子不会水解;
④pH试纸在使用之前不能用蒸馏水润湿.
②在金属晶体中,存在金属阳离子和自由移动的电子;
③铁离子在溶液中要水解,但是钠离子不会水解;
④pH试纸在使用之前不能用蒸馏水润湿.
解答:
解:①氯化铝是共价化合物,熔融氯化铝不含自由移动的铝离子,电解熔融的氧化铝来制取金属铝,故错误;
②晶体中有阳离子,未必一定有阴离子,如:在金属晶体中,存在金属阳离子和自由移动的电子,故错误;
③铁离子在溶液中要水解,1mol?L-1的FeCl3溶液每升中含有Fe3+小于1mol,故错误;
④pH试纸在使用之前不能用蒸馏水润湿,否则测定的是稀释以后溶液的pH值,但是弱测定纯水的pH时,不会影响结果,故错误.
故选D.
②晶体中有阳离子,未必一定有阴离子,如:在金属晶体中,存在金属阳离子和自由移动的电子,故错误;
③铁离子在溶液中要水解,1mol?L-1的FeCl3溶液每升中含有Fe3+小于1mol,故错误;
④pH试纸在使用之前不能用蒸馏水润湿,否则测定的是稀释以后溶液的pH值,但是弱测定纯水的pH时,不会影响结果,故错误.
故选D.
点评:本题涉及金属的冶炼、盐的水解、pH试纸的使用以及晶体的构成微粒等知识,注意知识的归纳和整理是关键,难度中等.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
与Li<Na<K<Rb<Cs的变化规律不符合的是( )
| A、与水或酸反应置换氢气越来越剧烈 |
| B、对应元素的金属性由弱到强 |
| C、对应金属阳离子氧化性由弱到强 |
| D、原子半径由小到大 |
下列实验操作或方法合理的是( )
| A、用加热NH4Cl的方法制氨气 |
| B、将CuSO4?5H2O置于蒸发皿中加热除去结晶水 |
| C、用金属钠检验酒精中是否含有水 |
| D、用饱和FeCl3溶液和沸水反应制备Fe(OH)3胶体 |
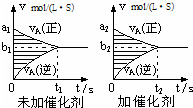 对于可逆反应mA(g)+nB(g)?pC(g)+qD(g),若其它条件都不变,探究催化剂对反应的影响,可得到如下两种v-t图象.下列判断正确的是( )
对于可逆反应mA(g)+nB(g)?pC(g)+qD(g),若其它条件都不变,探究催化剂对反应的影响,可得到如下两种v-t图象.下列判断正确的是( )| A、b1>b2,t1>t2 |
| B、两图中阴影部分面积一定相等 |
| C、A的平衡转化率(Ⅱ)大于(Ⅰ)中A的转化率 |
| D、若m+n<p+q,则压强变化对正反应速率的影响程度比逆反应速率影响程度大 |
下列说法错误的是( )
| A、向蛋白质溶液中加入CuSO4溶液发生蛋白质变性 |
| B、煤焦油中含有苯、二甲苯等化工原料 |
| C、天然气和可燃冰的主要成分都是甲烷 |
| D、石油裂解的主要目的是为了得到更多的汽油 |
下列说法正确的是( )
| A、葡萄糖与果糖、淀粉与纤维素均互为同分异构体 |
| B、纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 |
| C、糖、油脂、蛋白质均不溶于水 |
| D、淀粉、纤维素、蛋白质都是天然高分子化合物 |