题目内容
12.在下列溶液中,一定能大量共存的离子组是( )| A. | 常温下$\frac{c({H}^{+})}{c({OH}^{-})}$=1012的溶液中:Fe2+、Mg2+、NO3-、Cl- | |
| B. | 含有大量Al3+的溶液中:Na+、NH4+、Cl-、HCO3- | |
| C. | 能使pH试纸显蓝色的溶液中:K+、Ba2+、Cl-、Br- | |
| D. | 常温下,由水电离出的c(H+)=1×10-13 mol•L-1的溶液中:K+、Fe3+、CH3COO-、SO42-电解 |
分析 A.常温下$\frac{c({H}^{+})}{c({OH}^{-})}$=1012的溶液中呈酸性,硝酸根离子在酸性条件下能够氧化亚铁离子;
B.铝离子与碳酸氢根离子发生双水解反应;
C.能使pH试纸显蓝色的溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氢氧根离子反应;
D.该溶液中存在大量氢离子或氢氧根离子,铁离子与氢氧根离子反应,醋酸根离子与氢离子反应.
解答 解:A.常温下$\frac{c({H}^{+})}{c({OH}^{-})}$=1012的溶液中存在大量氢离子,Fe2+离子具有还原性,NO3-离子在酸性条件下具有强氧化性,二者发生氧化还原反应而不能大量共存,故A错误;
B.Al3+、HCO3-之间发生双水解反应,在溶液中不能大量共存,故B错误;
C.能使pH试纸显蓝色的溶液中存在大量氢氧根离子:K+、Ba2+、Cl-、Br-之间不发生反应,都不与氢氧根离子反应,在溶液中能够大量共存,故C正确;
D.常温下,由水电离出的c(H+)=1×10-13 mol•L-1的溶液中存在大量氢离子或氢氧根离子,CH3COO-与氢离子反应,Fe3+与氢氧根离子反应,在溶液中一定不能大量共存,故D错误;
故选C.
点评 本题考查离子共存,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列除去杂质的方法不正确的是( )
| A. | 镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 | |
| B. | 用过量氨水除去Fe3+溶液中的少量Al3+ | |
| C. | 加入新制的生石灰,再加热蒸馏,可以除去乙醇中的少量水 | |
| D. | Mg(OH)2中混有少量Al(OH)3,加入足量烧碱溶液,充分反应,过滤 |
17.称量一定体积的液体常用的玻璃仪器是( )
| A. | 试管 | B. | 量筒 | C. | 广口瓶 | D. | 锥形瓶 |
4.已知SO32-的还原性比I-强.某无色溶液可能含有I-、Fe3+、Na+、SO32-四种离子中的一种或几种,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于该溶液组成的判断正确的是( )
①肯定不含Fe3+;②肯定含I-;③可能含I-;④肯定含SO32-;⑤肯定含Na+;⑥可能含Na+.
①肯定不含Fe3+;②肯定含I-;③可能含I-;④肯定含SO32-;⑤肯定含Na+;⑥可能含Na+.
| A. | ①③④ | B. | ③④⑥ | C. | ①②④ | D. | ①③④⑤ |
1.“泰诺林”是治疗感冒发烧的一种药物.其主要成份的结构简式如下: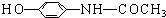 下列关于该物质的描述,不正确的是( )
下列关于该物质的描述,不正确的是( )
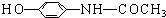 下列关于该物质的描述,不正确的是( )
下列关于该物质的描述,不正确的是( )| A. | 该化合物分子式为C8H9O2N | |
| B. | 能和银氨溶液发生银镜反应 | |
| C. | 能和氢氧化钠发生反应 | |
| D. | 其分子中的原子不可能都在同一平面上 |
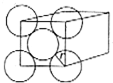 金晶体是面心立方最密堆积,立方体的每个面上5个金原子紧密堆砌(如图,其余各面省略),金原子半径为A cm,求:
金晶体是面心立方最密堆积,立方体的每个面上5个金原子紧密堆砌(如图,其余各面省略),金原子半径为A cm,求: .一定条件下,硫与地壳中含量最多的非金属元素X可组成两种常见的化合物,则X是O,两种化合物均含有的化学键为共价键
.一定条件下,硫与地壳中含量最多的非金属元素X可组成两种常见的化合物,则X是O,两种化合物均含有的化学键为共价键