题目内容
20.汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)?2NO(g)△H>0,已知该反应在2 404℃,平衡常数K=64×10-4.请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟后O2的物质的量为0.5mol,则N2的反应速率为0.05mol/(L•min).
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志AD.
A.消耗1mol N2同时生成1mol O2
B.断裂1NA个O=O键同时断裂1NA 个 N=O键
C.混合气体平均相对分子质量不变
D.2v正(N2)=v逆(NO)
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,如图变化趋势正确的是AC(填字母序号).

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态.与原平衡状态相比,此时平衡混合气中NO的体积分数不变.(填“变大”、“变小”或“不变”)
(5)在温度2 404℃条件下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1 mol/L、4.0×10-2 mol/L和3.0×10-3 mol/L,此时反应向正反应方向进行(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是因为浓度商Qc<K.
分析 (1)5分钟内,△n(O2)=1mol-0.5mol=0.5mol,由N2(g)+O2(g)?2NO(g)可知△n(N2)=0.5mol,带入v=$\frac{△n}{V•△t}$计算;
(2)可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析;
(3)根据温度、催化剂对反应速率和平衡移动的影响判断;
(4)根据化学方程式的特点结合压强对平衡的影响分析;
(5)计算某时刻生成物的浓度幂之积与反应物浓度幂之积的比值,与该温度下的平衡常数相比较,可得出结论.
解答 解:(1)5分钟内,△n(O2)=1mol-0.5mol=0.5mol,由N2(g)+O2(g)?2NO(g)可知△n(N2)=0.5mol,v(N2)═$\frac{△n}{V•△t}$=$\frac{0.5mol}{2L×5min}$=0.05mol/(L•min),
故答案为:0.05mol/(L•min);
(2)A.消耗1mol N2等效于消耗1mol O2,同时生成1mol O2,故选;
B.断裂1NA个O=O键同时断裂1NA 个 N=O键,正逆反应速率不相等,故不选;
C.混合气体平均相对分子质量不变,总质量是个定值,总物质的量是个定值,混合气体的平均相对分子质量一直不变,故不选;
D.2v(N2)正=v(NO)正=v(NO)逆,故选;
故选:AD;
(3)A、该反应的正反应为吸热反应,则升高温度平衡向正反应进行,平衡常数增大,故A正确;
B、加入催化剂,反应速率增大,但平衡不发生移动,故B错误;
C、升高温度,反应速率增大,平衡向正反应方向移动,氮气的转化率增大,故C正确.
故答案为:AC;
(4)该反应中,气体的化学计量数之和前后相等,压强对平衡移动没有影响,只要是在相同温度下,则平衡状态相同,与原平衡状态相比,此时平衡混合气中NO的体积分数,
故答案为:不变;
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,则有该时刻生成物的浓度幂之积与反应物浓度幂之积的比值为:$\frac{(3×10{\;}^{-3})^{2}}{(2.5×10{\;}^{-1})×(4.0×1{\;}^{-2})}$=9×10-4<K,则反应应向正反应方向进行,
故答案为:向正反应方向进行;因为浓度商Qc<K.
点评 本题考查化学平衡的有关计算,题目难度中等,注意平衡常数的计算和应用.

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案| A. |  | B. |  | C. |  | D. | 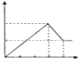 |
| A. | 使甲基橙变红的溶液中:Na+、Cl-、CH3COO-、Fe2+ | |
| B. | 水电离的OH-浓度为10-12mol/L-1的溶液中:Mg2+、NH4+、AlO2-、SO32- | |
| C. | 无色溶液中:Al3+、NO3-、Cl-、SO42- | |
| D. | c(H2C2O4)=0.5 mol/L溶液中:Na+、K+、MnO4-、Cl- |

| A. | 溶液B中发生的反应为:2SO2+O2→2SO3 | |
| B. | 由反应过程可推知氧化性:O2>Fe3+>SO42- | |
| C. | 溶液的pH:A>B>C | |
| D. | A溶液到C溶液,Fe3+浓度变大 |
| A. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 硝酸银溶液中加入铁粉:Ag++Fe═Fe2++Ag | |
| C. | 氧化铜与盐酸反应:O2-+2H+═H2O | |
| D. | 碳酸镁与稀硫酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
| A. | 氯分子的电子式: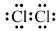 | |
| B. | 氯离子(Cl-)的结构示意图: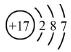 | |
| C. | 质子数为17、中子数为20的氯原子:${\;}_{17}^{20}Cl$ | |
| D. | 氯乙烯分子的结构简式:H3C-CH2Cl |
| A. | 放电过程中电解质溶液中阴离子移向正极 | |
| B. | 放电时每转移0.5mol电子,负极有0.5molV2+被氧化 | |
| C. | 充电时阳极附近溶液的酸性减弱 | |
| D. | 充电时阳极反应式为:VO2++2H++e-═VO2++H2O |