题目内容
8.钢铁是制造铁路、桥梁、轮船等的主要材料,钢铁在潮湿的空气中生锈时主要发生吸氧腐蚀(填“吸氧”或“析氢”),腐蚀时Fe作为原电池的负极,正极的电极反应为O2+4e-+2H2O=4OH-.分析 钢铁在潮湿的空气中,根据水膜为中性或弱酸性来分析发生的腐蚀的类型;在形成的原电池中,由于铁比碳活泼,据此分析正负极;若水膜显酸性,则发生析氢腐蚀,据此分析正负极反应.
解答 解:钢铁在潮湿的空气中,由于水膜为中性或弱酸性,故发生吸氧腐蚀;在形成的原电池中,由于铁比碳活泼,故铁做负极,负极反应为Fe-2e-=Fe2+,碳做正极,发生反应为:O2+4e-+2H2O=4OH-; 故答案为:吸氧;负;O2+4e-+2H2O=4OH-.
点评 本题考查了电化学腐蚀中的吸氧腐蚀和析氢腐蚀发生的条件,难度不大,应注意的是正负极反应的书写.

练习册系列答案
相关题目
18.X和Y均是短周期元素,它们之间可形成化合物X2Y3.若已知 X的原子序数为n,则Y的原子序数不可能是( )
| A. | n+1 | B. | n-5 | C. | n+3 | D. | n+6 |
16.常温常压下,下列各组气体能共存的是( )
| A. | SO2与O2 | B. | NO与O2 | C. | H2S与NO2 | D. | NH3和HCl |
13.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是( )
| A. | W、Y、Z的非金属性大小顺序一定是Z>Y>W | |
| B. | W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z | |
| C. | W、Z形成的某化合物常可用作萃取剂 | |
| D. | WY2分子中既有非极性键又有极性键 |
20.常温下,下列各环境下的离子组合能大量共存的是( )
| A. | 中性溶液中:Mg2+、Fe3+、SO42-、Cl- | |
| B. | 水电离出的c(OH-)=10-10mol•L-1:Al3+、NH4+、Ca2+、NO3- | |
| C. | c(H+)=10-14 mol•L-1 的溶液中:Na+、AlO2-、S2-、SO32- | |
| D. | pH试纸变红的溶液中:Fe3+、I-、NO3-、ClO- |
18.a、b、c、d为原子序数依次增大的短周期主族元素,其最外层电子数之和为20,a是第二周期元素,c原子最外层电子数既是a原子内层电子总数的3倍,又是b原子最外层电子数的2倍,下列说法正确的是( )
| A. | 原子半径:d>b | |
| B. | 最高价氧化物对应水化物的酸性:d>c | |
| C. | 化合物ac2中含有离子键 | |
| D. | 氧元素分别与a、b形成的化合物都是共价化合物 |
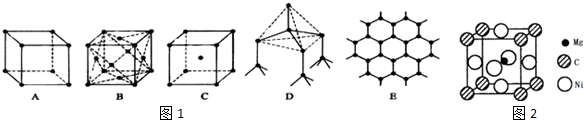
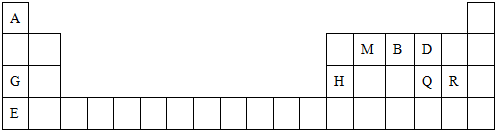
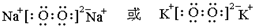 ;最高价氧化物的水化物中,酸性最强的化合物分子式为HClO4.
;最高价氧化物的水化物中,酸性最强的化合物分子式为HClO4.