题目内容
某氯化铁样品含有少量FeCl3杂质.现要测定其中铁元素的质量分数,实验按以下步骤进行: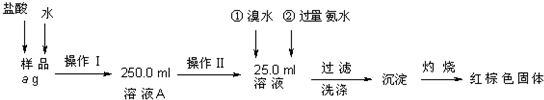
请根据上面流程回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须有 , (填仪器名称).
(2)请写出加入溴水发生反应的离子反应方程式: .
(3)检验沉淀是否已经洗涤干净的操作是: .
(4)该实验中可以回收利用的物质是 .
(5)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是 (列出算式,不需要化简);若称量准确,最终测量结果偏大,则造误差的原因可能是 .
(6)为进一步探究样品的性质,他们又利用溶液A做了如下一些实验,其中现象、结论均正确的是 (填写序号).
A向氢氧化镁悬浊液中滴加A溶液出现红褐色沉淀,证明Ksp[Fe(OH)3]<Ksp[Mg(OH)2)]
B向A溶液中加入少量铁粉,铁粉溶解,溶液颜色由黄色变成浅绿色.
C向沸水中滴加A的饱和溶液,立即出现红褐色沉淀.
D将A溶液加热蒸干并灼烧,得到Fe2O3固体.

请根据上面流程回答以下问题:
(1)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须有
(2)请写出加入溴水发生反应的离子反应方程式:
(3)检验沉淀是否已经洗涤干净的操作是:
(4)该实验中可以回收利用的物质是
(5)若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是
(6)为进一步探究样品的性质,他们又利用溶液A做了如下一些实验,其中现象、结论均正确的是
A向氢氧化镁悬浊液中滴加A溶液出现红褐色沉淀,证明Ksp[Fe(OH)3]<Ksp[Mg(OH)2)]
B向A溶液中加入少量铁粉,铁粉溶解,溶液颜色由黄色变成浅绿色.
C向沸水中滴加A的饱和溶液,立即出现红褐色沉淀.
D将A溶液加热蒸干并灼烧,得到Fe2O3固体.
考点:探究物质的组成或测量物质的含量,铁的氧化物和氢氧化物
专题:几种重要的金属及其化合物
分析:(1)配制一定物质的量浓度的溶液所需要的仪器有:量筒、胶头滴管、烧杯、玻璃棒、一定规格的容量瓶;根据操作II为滴定操作,必须用滴定管;
(2)Br2具有氧化性,能氧化Fe2+;为了使Fe3+充分沉淀,氨水要过量;
(3)取少量最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净;
(4)试验中生成的NH4Cl和NH4Br都可以回收利用;
(5)铁元素质量守恒,即红棕色固体( Fe2O3)中的铁就是样品中铁,根据质量分数的公式求出铁元素的质量分数;根据氢氧化铁固体加热时未充分反应变为Fe2O3;
(6)A.向氢氧化镁悬浊液中滴加A溶液出现红褐色沉淀,沉淀向溶度积小的转化,证明Ksp[Fe(OH)3]<Ksp[Mg(OH)2)];
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色由黄色变成浅绿色,说明Fe3+氧化铁粉;
C.向沸水中滴加A的饱和溶液,立即出现红褐色胶体;
D.将A溶液加热蒸干并灼烧,氢氧化铁沉淀分解生成得到Fe2O3固体.
(2)Br2具有氧化性,能氧化Fe2+;为了使Fe3+充分沉淀,氨水要过量;
(3)取少量最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净;
(4)试验中生成的NH4Cl和NH4Br都可以回收利用;
(5)铁元素质量守恒,即红棕色固体( Fe2O3)中的铁就是样品中铁,根据质量分数的公式求出铁元素的质量分数;根据氢氧化铁固体加热时未充分反应变为Fe2O3;
(6)A.向氢氧化镁悬浊液中滴加A溶液出现红褐色沉淀,沉淀向溶度积小的转化,证明Ksp[Fe(OH)3]<Ksp[Mg(OH)2)];
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色由黄色变成浅绿色,说明Fe3+氧化铁粉;
C.向沸水中滴加A的饱和溶液,立即出现红褐色胶体;
D.将A溶液加热蒸干并灼烧,氢氧化铁沉淀分解生成得到Fe2O3固体.
解答:
解:(1)因配制一定物质的量浓度的溶液所需要的仪器有:量筒、胶头滴管、烧杯、玻璃棒、一定规格的容量瓶;因操作II为滴定操作,必须用滴定管,
故答案:250mL容量瓶、量筒;
(2)因Br2具有氧化性,能氧化Fe2+:2Fe2++Br2=2Fe3++2Br-;为了使Fe3+充分沉淀,氨水要过量;故答案为:2Fe2++Br2=2Fe3++2Br-;使Fe3+充分沉淀;
(3)因最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,可证明洗涤干净,故答案为:取少量最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净;
(4)试验中生成的NH4Cl和NH4Br都可以回收利用,故答案为:NH4Cl和NH4Br;
(5)因铁元素质量守恒,即红棕色固体中的铁就是样品中铁,Fe2O3中铁元素的质量为(W2-W1)g×
,样品中铁元素的质量分数是
×100%;
故答案为:
×100%;
(6)A.向氢氧化镁悬浊液中滴加A溶液出现红褐色沉淀,沉淀向溶度积小的转化,证明Ksp[Fe(OH)3]<Ksp[Mg(OH)2)],故A正确;
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色由黄色变成浅绿色,说明Fe3+氧化铁粉,故B正确;
C.向沸水中滴加A的饱和溶液,立即出现红褐色胶体,故C错误;
D.将A溶液加热蒸干并灼烧,氢氧化铁沉淀分解生成得到Fe2O3固体,故D正确;
故答案为:ABD.
故答案:250mL容量瓶、量筒;
(2)因Br2具有氧化性,能氧化Fe2+:2Fe2++Br2=2Fe3++2Br-;为了使Fe3+充分沉淀,氨水要过量;故答案为:2Fe2++Br2=2Fe3++2Br-;使Fe3+充分沉淀;
(3)因最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,可证明洗涤干净,故答案为:取少量最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净;
(4)试验中生成的NH4Cl和NH4Br都可以回收利用,故答案为:NH4Cl和NH4Br;
(5)因铁元素质量守恒,即红棕色固体中的铁就是样品中铁,Fe2O3中铁元素的质量为(W2-W1)g×
| 112 |
| 160 |
| 112(W2-W1) |
| 160a |
故答案为:
| 112(W2-W1) |
| 160a |
(6)A.向氢氧化镁悬浊液中滴加A溶液出现红褐色沉淀,沉淀向溶度积小的转化,证明Ksp[Fe(OH)3]<Ksp[Mg(OH)2)],故A正确;
B.向A溶液中加入少量铁粉,铁粉溶解,溶液颜色由黄色变成浅绿色,说明Fe3+氧化铁粉,故B正确;
C.向沸水中滴加A的饱和溶液,立即出现红褐色胶体,故C错误;
D.将A溶液加热蒸干并灼烧,氢氧化铁沉淀分解生成得到Fe2O3固体,故D正确;
故答案为:ABD.
点评:本题主要考查了铁元素的质量分数的测定,同时考查了实验知识,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组中两种物质发生变化时,所克服的作用力属于同种类型的是( )
| A、二氧化硅和氯化镁熔化 |
| B、碘和氯化铵受热变成气体 |
| C、钠和硫受热变成气体 |
| D、氯化钠和硝酸钠溶于水 |
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、1mol Na2SO4溶于水中,所得溶液中Na+个数为NA |
| B、18g水含有电子数为8NA |
| C、标准状况下,22.4L氢气含有氢原子个数为2NA |
| D、22.4L氢气一定含有NA 个氢分子 |
下列电子式中,书写正确的是( )
A、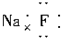 |
B、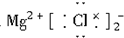 |
C、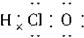 |
D、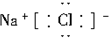 |
下列各种变化中,不属于化学变化的是( )
| A、加热胆矾得到白色的无水硫酸铜粉末 |
| B、向鸡蛋溶液中滴入饱和硫酸钠溶液,析出白色沉淀 |
| C、向沸水中滴入饱和氯化铁溶液,制取氢氧化铁胶体 |
| D、钢铁厂用热还原法冶炼铁 |
已知Mg(OH)2和Al(OH)3是工业上常用的阻燃剂,Mg(OH)2的分解温度范围为340~490℃,氢氧化铝的分解温度范围为190~230℃,它们的热化学方程式分别为:
Mg(OH)2(s)=MgO(s)+H2O(g)△H1=+81.5kJ?mol-1
Al(OH)3(s)=
Al2O3(s)+
H2O(g)△H2=+87.7kJ?mol-1
下列说法不正确的是( )
Mg(OH)2(s)=MgO(s)+H2O(g)△H1=+81.5kJ?mol-1
Al(OH)3(s)=
| 1 |
| 2 |
| 3 |
| 2 |
下列说法不正确的是( )
| A、Mg(OH)2和Al(OH)3高温下不分解,所以可做工业阻燃剂 |
| B、等质量Mg(OH)2和Al(OH)3相比,Mg(OH)2阻燃效果较好 |
| C、Mg(OH)2比Al(OH)3热稳定性高 |
| D、Mg(OH)2和Al(OH)3作为工业阻燃剂与它们分解吸热及生成物具有耐高温性有关 |
下列各组离子在指定条件下,一定能大量共存的是( )
| A、pH=1的无色溶液:Na+、Cu2+、NO3-、SO42- |
| B、能溶解Al(OH)3固体的溶液:K+、Na+、HCO3-、NO3- |
| C、能使碘化钾淀粉试纸变蓝的溶液:K+、Fe2+、SO42-、Cl- |
| D、水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、Cl-、NO3- |