题目内容
下列各组中两种物质发生变化时,所克服的作用力属于同种类型的是( )
| A、二氧化硅和氯化镁熔化 |
| B、碘和氯化铵受热变成气体 |
| C、钠和硫受热变成气体 |
| D、氯化钠和硝酸钠溶于水 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:
分析:原子晶体中需要克服共价键、分子晶体中需要克服分子间作用力、离子晶体中需要克服离子键,金属晶体需要克服金属键,根据晶体类型判断即可,据此分析解答.
解答:
解:A.二氧化硅属于原子晶体,需要克服化学键,氯化镁属于离子晶体,需要克服离子键,所以克服作用力不同,故A不选;
B.碘属于分子晶体,需要克服分子间作用力,氯化铵属于离子晶体,需要克服离子键,所以克服作用力不同,故B不选;
C.钠属于金属晶体,需要克服金属键,S属于分子晶体,需要克服分子间作用力,所以克服作用力不同,故C不选;
D.氯化钠和硝酸钠都属于离子晶体,溶于水都需要克服离子键,所以克服作用力相同,故D选;
故选D.
B.碘属于分子晶体,需要克服分子间作用力,氯化铵属于离子晶体,需要克服离子键,所以克服作用力不同,故B不选;
C.钠属于金属晶体,需要克服金属键,S属于分子晶体,需要克服分子间作用力,所以克服作用力不同,故C不选;
D.氯化钠和硝酸钠都属于离子晶体,溶于水都需要克服离子键,所以克服作用力相同,故D选;
故选D.
点评:本题考查化学键和晶体类型的关系,为高考高频点,明确晶体中存在的化学键是解本题关键,注意S是分子晶体不是原子晶体,为易错点.

练习册系列答案
相关题目
砹(At)是核电荷数最大的卤族元素,推测其单质及化合物最不可能具有的性质是( )
| A、单质砹是有色固体 |
| B、砹易与水反应 |
| C、HAt很不稳定 |
| D、砹易溶于某些有机溶剂 |
30℃时,在0.1mol/L的Na2S、NaHS两溶液中均存在的关系是( )
| A、c(H+)?c(OH-)<1×10-14 |
| B、c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| C、c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| D、c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) |
下列反应属于吸热反应的是( )
A、C6H12O6(葡萄糖aq)+6O2
| ||
| B、CH3COOH+KOH?CH3COOK+H2O | ||
| C、反应物的总能量大于生成物的总能量 | ||
| D、破坏反应物全部化学键所需能量大于破坏生成物全部化学键所需能量 |
下列关于各反应类型的关系中,说法正确的是( )
| A、置换反应一定属于氧化还原反应 |
| B、离子反应一定属于氧化还原反应 |
| C、有的复分解反应属于氧化还原反应 |
| D、所有化合反应都属于氧化还原反应 |
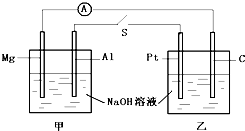 如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是( )| A、电流计指针不发生偏转 |
| B、Al、Pt两电极有氢气生成 |
| C、Mg、C两电极生成的气体在一定条件下可以恰好完全反应 |
| D、甲池pH减小,乙池pH不变 |