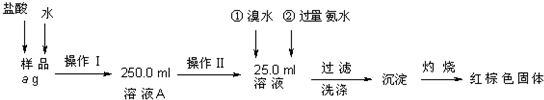
题目内容
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、1mol Na2SO4溶于水中,所得溶液中Na+个数为NA |
| B、18g水含有电子数为8NA |
| C、标准状况下,22.4L氢气含有氢原子个数为2NA |
| D、22.4L氢气一定含有NA 个氢分子 |
考点:阿伏加德罗常数
专题:
分析:A.1mol硫酸钠电离产生2mol钠离子;
B.1个水分子含有10个电子;
C.体积转化为物质的量,结合1个氢气分子含有2个氢原子解答;
D.没指明气体的状况,Vm不确定.
B.1个水分子含有10个电子;
C.体积转化为物质的量,结合1个氢气分子含有2个氢原子解答;
D.没指明气体的状况,Vm不确定.
解答:
解:A.1mol硫酸钠电离产生2mol钠离子,所以1mol Na2SO4溶于水中,所得溶液中Na+个数为2NA,故A错误;
B.1个水分子含有10个电子,18g水的物质的量为
,含有电子数为10NA,故B错误;
C.1个氢气分子含有2个氢原子,标准状况下,22.4L氢气的物质的量为
=1mol,含有氢原子个数为2NA,故C正确;
D.没指明气体的状况,Vm不确定,无法计算22.4L氢气的物质的量,故D错误;
故选:C.
B.1个水分子含有10个电子,18g水的物质的量为
| 18g |
| 18g/mol |
C.1个氢气分子含有2个氢原子,标准状况下,22.4L氢气的物质的量为
| 22.4L |
| 22.4L/mol |
D.没指明气体的状况,Vm不确定,无法计算22.4L氢气的物质的量,故D错误;
故选:C.
点评:本题考查阿伏加德罗常数,明确物质的组成,把握物质的量的相关计算公式的运用是解题关键,题目难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
30℃时,在0.1mol/L的Na2S、NaHS两溶液中均存在的关系是( )
| A、c(H+)?c(OH-)<1×10-14 |
| B、c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| C、c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| D、c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) |
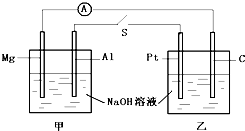 如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯用导线如图相连,Pt、Mg、A1、C分别为四个电极,当闭合开关S后,以下表述正确的是( )| A、电流计指针不发生偏转 |
| B、Al、Pt两电极有氢气生成 |
| C、Mg、C两电极生成的气体在一定条件下可以恰好完全反应 |
| D、甲池pH减小,乙池pH不变 |
下列说法正确的是( )
| A、摩尔是国际单位制中的七个物理量之一 |
| B、摩尔表示物质的量 |
| C、1mol任何物质都含有6.02×1023个原子 |
| D、1mol O2中有6.02×1023个氧分子 |
下列表示对应化学反应的离子方程式正确的是( )
| A、盐酸中加入碳酸钙:CO32-+2H+═H2O+CO2↑ |
| B、向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
准确量取25.00mL KMnO4溶液于锥形瓶中并用某无色未知浓度的还原性A溶液进行滴定,所选仪器和指示剂均正确的是( )
| A、50 mL酸式滴定管;甲基橙 |
| B、50 mL碱式滴定管;酚酞 |
| C、50 mL量筒;石蕊 |
| D、50 mL酸式滴定管;不用指示剂 |